
【题目】A、B、C、D、E、F六种元素位于短周期,原子序数依次增大,C基态原子核外有三个未成对电子,B与D形成的化合物BD与C的单质C2电子总数相等,CA3分子结构为三角锥形,D与E可形成E2D与E2D2两种离子化合物,D与F是同族元素。根据以上信息,回答下列有关问题:
(1)写出基态时D的电子排布图________。
(2)写出化合物E2F2的电子式________,化合物ABC的结构式________。
(3)根据题目要求完成以下填空:
①BF32﹣中心原子杂化方式________;CA3中心原子杂化方式________;
②FD42﹣微粒中的键角________; FD3分子的立体构型________。
(4)F元素两种氧化物对应的水化物酸性由强到弱为__________,原因__________________。
【答案】![]()
![]() H-C≡N sp2 sp3 109°28′ 平面三角形 H2SO4> H2SO3 H2SO4中非羟基氧原子个数比H2SO3多,酸性强
H-C≡N sp2 sp3 109°28′ 平面三角形 H2SO4> H2SO3 H2SO4中非羟基氧原子个数比H2SO3多,酸性强
【解析】
A、B、C、D、E、F六种元素位于短周期,原子序数依次增大,C基态原子核外有三个未成对电子,且C能形成单质C2 ,所以C是N元素;B与D形成的化合物BD与C2电子总数相等,且C的原子序数大于B小于D,所以B是C元素,D是O元素;CA3 分子结构为三角锥形,且A的原子序数小于B,所以A是H元素;D与E可形成E2D 与E2D2 两种离子化合物,所以E是Na元素;D与F是同族元素,所以F是S元素。根据上述分析进行解答。
(1)通过以上分析知,D是O元素,原子核外有8个电子,其核外电子排布图为![]() ,
,
故答案为:![]() ;
;
(2)E2F2 为Na2S2 ,和过氧化钠类似,所以其电子式为:![]() ;化合物ABC是氢氰酸,结构式为 H-C≡N ,
;化合物ABC是氢氰酸,结构式为 H-C≡N ,
故答案为:![]() ; H-C≡N ;
; H-C≡N ;
(3) ①BF32﹣为CS32-,和CO32-相似,中心原子C的价层电子对数=3+0=3,中心原子杂化方式sp2;CA3为NH3,中心原子N的价层电子对数=3+1=4,中心原子杂化方式sp3,
故答案为:sp2 ;sp3;
②FD42- 为SO42-, S的价层电子对数=4+0=4,所以它的VSEPR模型为正四面体,因为没有孤电子对,所以其空间构型为正四面体,键角是109°28′;FD3 为SO3 ,S的价层电子对数=3+0=3,所以它的VSEPR模型为平面三角形,因为没有孤电子对,所以其空间构型为平面三角形,
故答案为:109°28′ ;平面三角形;
(4) S元素两种氧化物对应的水化物为H2SO4和H2SO3,同一种元素含氧酸中,含有非羟基O原子个数越多,其酸性越强,硫酸中非羟基氧原子个数为2、亚硫酸中非羟基氧原子个数是1,所以硫酸酸性强于亚硫酸,
故答案为:H2SO4> H2SO3 ;H2SO4中非羟基氧原子个数比H2SO3多,酸性强。


科目:高中化学 来源: 题型:
【题目】氮氧化物和硫氧化物是常见的空气污染物,含氮氧化物和硫氧化物的尾气需处理后才能排放。
Ⅰ.氮氧化物的处理
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为_________。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为NO+NO2+2OH=2NO2-+H2O,2NO2+2OH= NO2-+NO3-+H2O,吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是_________(填化学式)。
(3)NO的氧化吸收。在酸性NaClO溶液中,HClO氧化NO生成Cl和NO3-。其他条件相同,NO转化为NO3-的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。NaClO溶液的初始pH越小,NO转化率越高。其原因是_________。
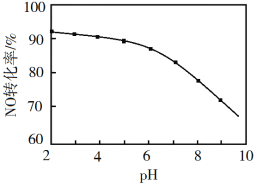
Ⅱ.煤燃烧排放的烟气中SO2和NOx的处理
采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有SO2和NOx的烟气,反应温度为323K,NaClO2溶液浓度为5×103mol·L1 。反应一段时间后溶液中离子浓度的分析结果如下表。
离子 | SO42 | SO32 | NO3 | NO2 | Cl |
c/(mol·L1) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
(4)写出NaClO2溶液脱硫过程中主要反应的离子方程式________。增加压强,NO的转化率_________(填“提高”“不变”或“降低”)。
(5)由实验结果可知,脱硫反应速率大于脱硝反应速率。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,100mL0.1mol·L-1 的H2A 溶液中滴加0.1mol·L-1NaOH溶液,含A元素相关微粒物质的量随pH的变化如图所示。下列说法正确的是
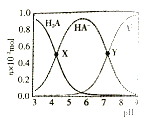
A.将等浓度等体积的Na2A与H2A溶液混合后,溶液显碱性
B.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
C.X 点溶液中含A元素的相关离子存在以下关系:c(H2A)+c(HA-)+c(A2-)=0.1mol·L-1
D.Y点溶液中存在以下关系:c(H+) +c(Na+)=c(OH-)+3c(HA-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质G是制备抗癌药物吉非替尼过程中重要的中间体,某研究小组按照下列线路合成中间体G。

已知: 、
、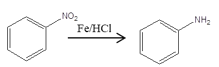 、
、 (同时还有H2O或卤化氢生成)
(同时还有H2O或卤化氢生成)
请回答:
(1)下列说法正确的是_______。
A.化合物A能够使酸性高锰酸钾溶液褪色
B.化合物A中含有4种不同的官能团
C.化合物C具有碱性
D.化合物G的分子式为C15H20N3O3
(2)上述路线中合成A的反应类型为______,化合物E的结构简式为______。
(3)写出C到D的化学反应方程式________。
(4)请设计以乙烯为原料转变为物质C的合成线路(用流程图表示,无机试剂任选)___。
(5)写出化合物B(C8H7NO2)可能的同分异构体_______。须同时满足:①能发生银镜反应;②1H—NMR谱显示分子中含有苯环,且分子中有4种不同化学环境的氢原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子。N4分子结构如图所示,下列说法正确的是( )
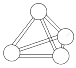
A. N4分子属于一种新型的化合物B. N4分子中只含有非极性键
C. 1 mol N4分子所含共价键数为4NAD. N4沸点比P4(白磷)高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是

A. 分子中含有2种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知烯烃经O3氧化后,在锌存在水解可得到醛或酮,现有分子式为C7H14的某烯烃,它与氢气发生加成反应生成2,3-二甲基戊烷,被臭氧氧化后在锌存在下水解生成乙醛和一种酮(![]() ):
):
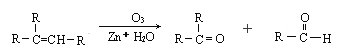
由此可推断该有机物的结构简式为( )
A. ![]() B.
B. 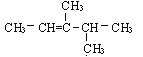
C. ![]() D. (CH3)2C=C(CH3)CH2CH3
D. (CH3)2C=C(CH3)CH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应NH4Cl+NaNO2![]() NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
A. 中子数为18的氯原子:![]()
B. N2的结构式:N=N
C. Na+的结构示意图: 
D. H2O的电子式: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用图示装置进行实验,反应进行足够长时间后装置II中实验现象正确的是
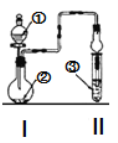
① | ② | ③ | II中实验现象 | |
A | 浓盐酸 | 大理石 | 氯化钡溶液 | 产生大量白色沉淀 |
B | 浓氨水 | 碱石灰 | 硫酸亚铁溶液 | 产生大量白色沉淀 |
C | 冰醋酸 | 乙醇和浓硫酸 | 饱和碳酸钠溶液 | 溶液分层,上层为油状液体 |
D | 浓盐酸 | KMnO4 | 氢硫酸 | 产生淡黄色沉淀 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com