
【题目】为了研究化学反应A+B===C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:
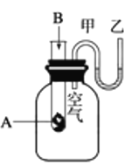
(1)该反应为____________反应(填“放热”或“吸热”)。
(2)反应物化学键断裂吸收的能量________(填“高”或“低”)于生成物化学键形成放出的能量。
(3)写出一个符合题中条件的化学方程式:_______________________
【答案】放热 低 2Al+6HCl===2AlCl3+3H2↑(或2Na+2H2O===2NaOH+H2↑或NaOH+HCl===NaCl+H2O等合理答案均可)
【解析】
试管中反应的热量变化与试管壁外的空气发生热量交换,广口瓶中的空气是我们研究的对象,再根据气体热胀冷缩的原理分析。
(1)因为“看到U形管中甲处液面下降乙处液面上升”,说明广口瓶中的空气体积增大,气压增大,这只能是A和B反应放出的热量传导给广口瓶中的空气造成的,由此推断A+B=C+D是放热反应;
(2)一个放热反应,一定是反应物断开化学键吸收的总能量小于生成物形成化学键释放的总能量,所以填“低”;
(3)所写化学方程式应符合:①常温常压下,两种反应物生成两种生成物;②放热反应。如2Al+6HCl==2AlCl3+3H2↑、2Na+2H2O==2NaOH+H2↑、NaOH+HCl==NaCl+H2O等。


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】已知K、Ka、Kw、Kh、Ksp分别表示化学平衡常数、弱酸的电离平衡常数、水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。
(1)25℃时,将a mol/L的氨水与0.01 mol/L的盐酸等体积混合所得溶液中,c(NH4+)=c(Cl-)则溶液显__________(填"酸""碱"或"中")性;用含a的代数式表示NH3·H2O的电离平衡常数Kb=__________;
(2)25℃,H2SO3![]() HSO3-+H+,其电离平衡常数Ka=1×10-2 mol/L,则该温度下pH=3,c(HSO3-)=0.1mol/L的NaHSO3溶液中c(H2SO3)=__________;
HSO3-+H+,其电离平衡常数Ka=1×10-2 mol/L,则该温度下pH=3,c(HSO3-)=0.1mol/L的NaHSO3溶液中c(H2SO3)=__________;
(3)高炉炼铁中发生的反应有:FeO(s)+CO(g)![]() Fe(s)+CO2(g) ΔH<0
Fe(s)+CO2(g) ΔH<0
①该反应的平衡常数表达式K=__________;
②已知1100℃时,K=0.25,则平衡时CO的转化率为__________;
③在该温度下,若测得高炉中c(CO2)=0.020mol/L,c(CO)=0.1 mol/L,则此时反应速率v正__________(填">""<"或"=")v逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉煤气是炼铁厂排放的尾气,含有H2、N2、CO、CO2及O2,其中N2约为55%、CO约为25%、CO2约为15%、O2约为1.64%(均为体积分数)。某科研小组对尾气的应用展开研究:
(1)直接作燃料
已知:C(s)+O2(g)![]() CO2 (g) ΔH=-393.5kJ/mol
CO2 (g) ΔH=-393.5kJ/mol
2C(s)+O2(g)![]() 2CO (g) ΔH=-221kJ/mol
2CO (g) ΔH=-221kJ/mol
CO燃烧热的热化学方程式为__________。
(2)生产合成氨的原料
高炉煤气经过下列步骤可转化为合成氨的原料气:

在脱氧过程中仅吸收了O2,交换过程中发生的反应如下,这两个反应均为吸热反应:
CO2+CH4![]() CO+H2(未配平) CO+H2O
CO+H2(未配平) CO+H2O![]() CO2+ H2
CO2+ H2
①气体通过微波催化交换炉需要较高温度,试根据该反应特征,解释采用较高温度的原因____________________________________________。
②通过铜催化交换炉后,所得气体中V(H2):V(N2)=__________。
(3)合成氨后的气体应用研究
①氨气可用于生产硝酸,该过程中会产生大气污染物NOx。为了研究对NOx的治理,该科研小组在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,发生如下反应:2NO(g)+Cl2(g)![]() 2ClNO(g) ΔH<0。10min时反应达平衡,测得10min内v(ClNO)=7.5×10-3mol/(L·min),则平衡后n(Cl2)=__________mol。设此时NO的转化率为α1,若其它条件不变,上述反应在恒压条件下进行,平衡时NO的转化率为α2,则α1__________α2 (填“>”、“<”或“=”);平衡常数K__________(填增大”“减小 ”或“不变”)
2ClNO(g) ΔH<0。10min时反应达平衡,测得10min内v(ClNO)=7.5×10-3mol/(L·min),则平衡后n(Cl2)=__________mol。设此时NO的转化率为α1,若其它条件不变,上述反应在恒压条件下进行,平衡时NO的转化率为α2,则α1__________α2 (填“>”、“<”或“=”);平衡常数K__________(填增大”“减小 ”或“不变”)
②氨气还可用于制备NCl3,NCl3发生水解产物之一具有强氧化性,该水解产物能将稀盐酸中的NaClO2氧化成ClO2,该反应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A. NaCl的摩尔质量是58.5g
B. 在1L水中溶解5.85gNaCl,即可配制得0.1mol/L的NaCl溶液
C. 标准状况下,22.4L H2O含有氢原子的数目为2NA
D. 17g NH3中含有分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A—E五种物质都含有同一种元素,它们之间的转化关系如图所示,其中A为淡黄色固体化合物,B为单质。
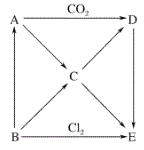
(1)固体A的名称为____,单质B的常见用途有:_____(任写一条)。
(2)写出下列反应的化学方程式
①B→C__________
②A→D__________
(3)写出将氯气通入C溶液中的化学方程式_____,其溶液有漂白作用,漂白原理是______。(写反应方程式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用VSEPR模型预测下列分子或离子的立体结构,其中正确的是 ( )
A. H2O与BeCl2为角形(V形) B. CS2与SO2为直线形
C. SO3与CO![]() 为平面三角形 D. BF3与PCl3为三角锥形
为平面三角形 D. BF3与PCl3为三角锥形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是有关钠与水反应及产物检验的实验装置。实验开始时先向管内加入滴有酚酞试液的水,使水位达到B端管口,然后迅速塞紧橡胶塞并拔掉大头针,此时Na掉入水中。回答下列问题:

(1)钠与水反应的化学方程式为_____________。
(2)钠与水反应的现象有很多,不同的现象证明不同的性质。
①能证明钠的密度比水小的现象是_________。
②能证明钠的熔点低的现象是_________。
③能证明有氢氧化钠生成的现象是__________。
④能证明有气体产生的现象是A端液面________(填“上升”“下降”或“不变”,下同),B端液面________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com