
 ���ڱ�����A��B��C����ԭ���������������Ԫ�أ�A�ǵؿ��к������Ľ���Ԫ�أ�B�ļ۲�����Ų�Ϊnsn-1npn+1��C�������е�һ�ֳ��ý�������ԭ�ӵ���Χ�����Ų�Ϊ3d104s1��
���ڱ�����A��B��C����ԭ���������������Ԫ�أ�A�ǵؿ��к������Ľ���Ԫ�أ�B�ļ۲�����Ų�Ϊnsn-1npn+1��C�������е�һ�ֳ��ý�������ԭ�ӵ���Χ�����Ų�Ϊ3d104s1������ ���ڱ�����A��B��C����ԭ���������������Ԫ�أ�A�ǵؿ��к������Ľ���Ԫ�أ���AΪAl��B�ļ۲�����Ų�Ϊnsn-1npn+1������s�ܼ��������2�����ӣ���p�ܼ����ɵ��ӣ���n=3����BΪSԪ�أ�C�������е�һ�ֳ��ý�������ԭ�ӵ���Χ�����Ų�Ϊ3d104s1����CΪCu��
��1��AΪAl�أ�ԭ�Ӻ�����13�����ӣ���Ϲ���ԭ����д��������Ų�ʽ��
��2��һ����̼��N2��Ϊ�ȵ����壬�ȵ�����ṹ���ƣ���CO�ĽṹʽΪC��O����������1���Ҽ���2���м���
��3���Զ���Cuԭ���о�������֮�Ⱦ��������Cuԭ��λ�����ģ���ÿ������Ϊ12���湲�ã�
��ͼ��֪��ÿ��Mԭ����Χ��6��Nԭ�ӣ���ÿ��Nԭ��Ϊ3��Mԭ�ӹ��ã��ݴ˼���M��Nԭ����Ŀ֮�ȣ�����ȷ����ѧʽ��
��4��B������������Ӧˮ����Ϊ���ᣬ���������£�Cu��Ũ���ᷴӦ��������ͭ������������ˮ��
��5��������ͭ��һˮ�ϰ���Ӧ����[Cu��NH3��4]��OH��2��ˮ��
��6������[CO��NH2��2]�ʹ������ơ�NaOH��Һ��Ӧ����������N2H4����Na2CO3��H2O��NaCl����ƽ��д����ʽ��
��� �⣺���ڱ�����A��B��C����ԭ���������������Ԫ�أ�A�ǵؿ��к������Ľ���Ԫ�أ���AΪAl��B�ļ۲�����Ų�Ϊnsn-1npn+1������s�ܼ��������2�����ӣ���p�ܼ����ɵ��ӣ���n=3����BΪSԪ�أ�C�������е�һ�ֳ��ý�������ԭ�ӵ���Χ�����Ų�Ϊ3d104s1����CΪCu��
��1��AΪAl�أ�ԭ�Ӻ�����13�����ӣ��ɹ���ԭ����֪��������Ų�ʽΪ1s22s22p63s23p1��
�ʴ�Ϊ��1s22s22p63s23p1��
��2��һ����̼��N2��Ϊ�ȵ����壬�ȵ�����ṹ���ƣ���CO�ĽṹʽΪC��O����������1���Ҽ���2���м���һ����̼�����ЦҼ���м���Ŀ֮��Ϊ1��2��
�ʴ�Ϊ��1��2��
��3���Զ���Cuԭ���о�����֮�Ⱦ��������Cuԭ��λ�����ģ���ÿ������Ϊ12���湲�ã�����Cuԭ�ӵȾ����������Cuԭ����12����
��ͼ��֪��ÿ��Mԭ����Χ��6��Nԭ�ӣ���ÿ��Nԭ��Ϊ3��Mԭ�ӹ��ã���ÿ��Nԭ��Ϊһ��Mԭ���ṩ$\frac{1}{3}$����M��Nԭ����Ŀ֮��Ϊ1��6��$\frac{1}{3}$=1��2����ѧʽΪMN2��
�ʴ�Ϊ��MN2��
��4��B������������Ӧˮ����Ϊ���ᣬ���������£�Cu��Ũ���ᷴӦ��������ͭ������������ˮ����Ӧ����ʽΪ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
�ʴ�Ϊ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
��5��������ͭ��һˮ�ϰ���Ӧ����[Cu��NH3��4]��OH��2��ˮ����Ӧ����ʽΪ��Cu��OH��2+4NH3��H2O=[Cu��NH3��4]��OH��2+4H2O��
�ʴ�Ϊ��Cu��OH��2+4NH3��H2O=[Cu��NH3��4]��OH��2+4H2O��
��6������[CO��NH2��2]�ʹ������ơ�NaOH��Һ��Ӧ����������N2H4����Na2CO3��H2O��NaCl���÷�Ӧ����ʽΪ��CO��NH2��2+NaClO+2NaOH=N2H4+Na2CO3+NaCl+H2O��
�ʴ�Ϊ��CO��NH2��2+NaClO+2NaOH=N2H4+Na2CO3+NaCl+H2O��
���� ���⿼���������Ų����ȵ����塢��ѧ�����������㡢����ʽ��д�ȣ��Ƕ�ѧ���ۺ������Ŀ��飬��3��ע�����þ�̯������ȷ����ѧʽ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Q1=Q2=Q3=57.3 | B�� | Q1��Q2��Q3��57.3 | C�� | Q3��Q1��Q2=57.3 | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
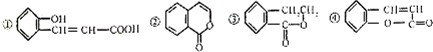
| A�� | ֻ�Т��ܺ�̼���Ʒ�Ӧ�ų����� | B�� | �ںܻ͢�Ϊͬ���칹�� | ||
| C�� | �٢ڢܶ�����ʹ��ˮ��ɫ | D�� | ����H2�ӳɺ���Եõ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ��ɫ��������Al��OH��3���������CO2��ԭ�������һ������Al3+��HCO3- | |
| B�� | ��ɫ��������BaSO4��ԭ�������һ������SO42- | |
| C�� | ������һ����NO��NO2�Ļ������ | |
| D�� | ԭ�������һ������Na+��Al3+��NO3-��SO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | �����ӻ���� | Ҫ�� |
| ��A | Mg2+��SO42-��Cl-��NO3- | ��c��Mg2+��=c��SO42-�� |
| ��B | Na+��Cu2+��I-��NH3•H2O | �����Ը��������Һ�� |
| ��C | NH4+��Al3+��Cl-��NO3- | ���μӰ�ˮ�г������� |
| ��D | Cl-��Na+��Cr2O72-��C2H5OH | ����Һ��ɫ�����������Ժ�ɫ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ӵİ뾶��r��A����r��C����r��D����r��E�� | |
| B�� | Ԫ��B�������̬��������ȶ��Ա�C��ǿ | |
| C�� | D2C2��A2C2��Ư��ԭ����ͬ | |
| D�� | Ԫ��E��������������B��D������������Ӧ��ˮ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
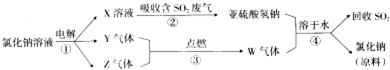
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6�� | B�� | 8�� | C�� | 10�� | D�� | 12�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 30.8% | B�� | 28.6% | C�� | 25.3% | D�� | 22.7% |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com