
| 选项 | 实验操作 | 实验现象 | 结 论 |
| A | 测定等浓度的Na2CO3和Na2SO3 溶液的pH | 前者pH比后者的大 | 非金属性:S>C |
| B | SO2通入酸性高锰酸钾溶液 | 高锰酸钾溶液褪色 | SO2具有还原性 |
| C | 溴乙烷与NaOH溶液共热后,加HNO3酸化的AgNO3溶液 | 出现淡黄色沉淀 | 溴乙烷发生了水解 |
| D | 向等浓度的KBr、KI混合液中滴加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgBr)>Ksp(AgI) |
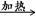 CH3CH2OH+NaBr。再加入HNO3酸化的AgNO3溶液时发生Br-+Ag+=AgBr↓。证明溴乙烷在NaOH的水溶液中发生了水解反应。正确。D.物质越难溶,反应产生沉淀所需要的离子的浓度就越小,就越先反应得到沉淀。Br-+Ag+=AgBr↓;AgBr是淡黄色沉淀,I-+Ag+=AgI↓,AgI是黄色沉淀。向等浓度的KBr、KI混合液中滴加AgNO3溶液,先出现黄色沉淀说明先发生反应I-+Ag+=AgI↓。因此Ksp(AgBr)>Ksp(AgI)。正确。2、溴乙烷的化学性质的知识。
CH3CH2OH+NaBr。再加入HNO3酸化的AgNO3溶液时发生Br-+Ag+=AgBr↓。证明溴乙烷在NaOH的水溶液中发生了水解反应。正确。D.物质越难溶,反应产生沉淀所需要的离子的浓度就越小,就越先反应得到沉淀。Br-+Ag+=AgBr↓;AgBr是淡黄色沉淀,I-+Ag+=AgI↓,AgI是黄色沉淀。向等浓度的KBr、KI混合液中滴加AgNO3溶液,先出现黄色沉淀说明先发生反应I-+Ag+=AgI↓。因此Ksp(AgBr)>Ksp(AgI)。正确。2、溴乙烷的化学性质的知识。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2O和Na2O2组成元素相同,与CO2反应产物也相同 |
| B.SO2和CO2都是酸性氧化物,都能与NaOH溶液反应 |
| C.NO和NO2的密度均比空气大,都可用向上排空气法收集 |
| D.C3H8和CH3CH2OH相对分子质量相近,分子间作用力相近,二者沸点也相近 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铜与浓硫酸共热,产生使石蕊溶液变红的气体,说明浓硫酸具有酸性 |
| B.将金属钠投入冷水中,钠熔为小球,说明钠与水的反应为放热反应且钠的熔点低 |
| C.向AgCl浊液中滴加Na2S溶液,白色沉淀变成黑色,说明AgCl的溶解平衡正向移动 |
| D.向Al(OH)3沉淀中滴加NaOH溶液或盐酸,沉淀均消失,说明Al(OH)3是两性氢氧化物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
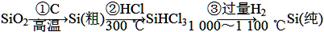
| 物质 | SiHCl3 | SiCl4 | HCl |
| 沸点 | 33.0 ℃ | 57.6 ℃ | -84.7 ℃ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 陈述I | 陈述II |
| A | SO2有漂白性 | SO2能使紫色石蕊试液褪色 |
| B | 浓硫酸具有吸水性和强氧化性 | 将浓硫酸滴到用水润湿的蔗糖中,蔗糖变黑色海绵状 |
| C | 在一定条件下铁与水可以发生反应 | 将水蒸气通过灼热的铁粉,粉末变红 |
| D | 盐类水解都是吸热反应 | 向0.1mol·L-1 Na2CO3溶液中,滴加2滴酚酞显浅红色,微热,红色加深。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若以w1和w2分别表示浓度为amol·L-1和bmol·L-1氨水的质量分数,且知2a=b,则w2>2w1(氨水的密度比纯水的小) |
| B.7.8gNa2O2与CO2完全反应,转移0.2mol电子 |
| C.CO2、SO3、NO2和水反应均能生成酸,都属于酸性氧化物 |
| D.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.FeCl2、Na2O2、NaHCO3均可通过化合反应生成 |
| B.在稀硫酸中加入铜粉,铜粉不溶解,若加入KNO3固体,铜粉溶解 |
| C.用渗析的方法可除去Fe(OH)3胶体中混有的Cl- |
| D.氧化铝具有高熔点,用氧化铝制作的坩埚可用来蒸发浓缩烧碱溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com