
A、用两根铜棒电解盐酸:2H++2Cl-
| ||||
| B、14g乙烯燃烧生成液态水产生b kJ热量,则表示其燃烧热的热化学方程式为:C2H4(g)+3O2(g)═2H2O(g)+2CO2(g)△H=-2b kJ?mol-1 | ||||
| C、向Ca(OH)2溶液中加入过量的NaHCO3溶液:Ca2++HCO3-+OH-=CaCO3↓+2H2O | ||||
| D、在酸性碘化亚铁溶液中通入少量氧气:4I-+O2+4H+=2I2+2H2O |
| ||


 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
| ||
| A、电解时,石墨作阳极,不锈钢作阴极 |
| B、电解时的阳极电极反应式:I--6e-+3H2O=IO3-+6H+ |
| C、当电解过程中转移3 mol e-时,理论上可制得KIO3 107 g |
| D、电解一段时间后,电解质溶液的pH变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在化学反应过程中,吸热反应需不断从外界获得能量,放热反应不需从外界获得能量 |
| B、甲烷的燃烧热△H=-890kJ/mol,则甲烷燃烧的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890kJ?mol-1 |
| C、已知常温常压下:HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ?mol-1,则有:H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)△H=-114.6 kJ?mol-1 |
| D、已知:S(s)+O2(g)=SO2(g)△H1=-Q1 kJ?mol-1,S(g)+O2(g)=SO2(g)△H2=-Q2kJ?mol-1,则Q1<Q2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、自然界中的一切物质的能量均来自太阳 |
| B、人体每摄入1摩尔葡萄糖,就为人体提供2870kJ能量 |
| C、人体所需的能量均来自于葡萄糖的氧化 |
| D、1摩尔固态葡萄糖和6摩尔氧气所含能量大于6摩尔CO2和6摩尔液态水所含的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
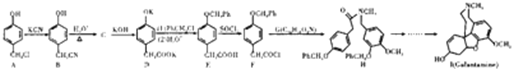
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com