
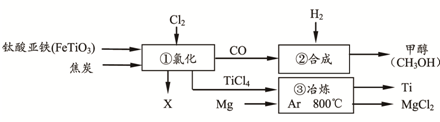
分析 FeTiO3和焦炭在加热条件下通入氯气发生氧化还原反应生成TiCl4、FeCl3和CO,生成的CO和氢气可在一定条件下生成甲醇,TiCl4和Mg在Ar的氛围中加热至800℃可生成Ti和MgCl2,
(1)在物质的组成中含有碳元素的化合物叫有机物,但是一氧化碳、二氧化碳、碳酸钙等具有无机物的性质,属于无机物;
(2)根据质量守恒定律判断;
(3)反应③是四氯化钛和镁在高温的条件下生成氯化镁和钛;
(4)一氧化碳和氢气合成乙醇,反应的方程式为CO+2H2=CH3OH,结合方程式判断.
解答 解:FeTiO3和焦炭在加热条件下通入氯气发生氧化还原反应生成TiCl4、FeCl3和CO,生成的CO和氢气可在一定条件下生成甲醇,TiCl4和Mg在Ar的氛围中加热至800℃可生成Ti和MgCl2,
(1)该流程图中涉及到的物质中属于有机物的只有甲醇,故答案为:甲醇(CH3OH);
(2)根据质量守恒定律可知,在化学反应前后原子个数不变,所以X是FeCl3,故答案为:FeCl3;
(3)反应③是四氯化钛和镁在高温的条件下生成氯化镁和钛,单质和化合物反应生成单质和化合物,属于置换反应,故答案为:置换;
(4)一氧化碳和氢气合成乙醇,方程式为CO+2H2=CH3OH,为使原料全部转化为甲醇,理论上CO和H2投料的质量比为28:4=7:1,故答案为:7:1.
点评 本题以流程图的形式考查物质的制备,为高频考点,需要学生具备综合运用知识及题目信息分析问题、解决问题能力.对于这类题目,需要搞清楚每一步反应物、生成物,清楚工艺流程原理,题目难度中等.


科目:高中化学 来源: 题型:解答题
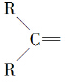 ”生成酮,“
”生成酮,“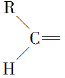 ”生成“
”生成“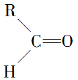 ”,
”,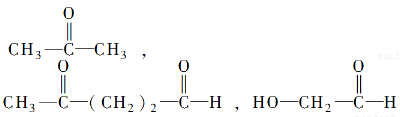
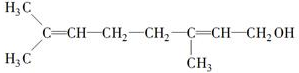 或
或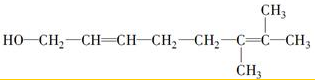 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
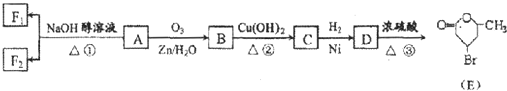
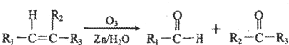
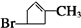
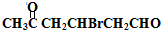 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$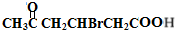 +Cu2O↓+2H2O
+Cu2O↓+2H2O .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
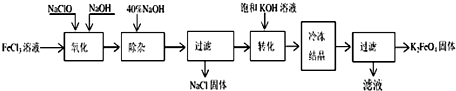
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
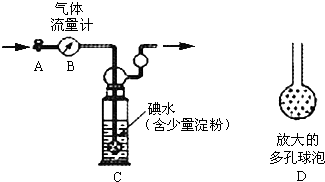 硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放.某校兴趣小组欲测定硫酸工业尾气中二氧化硫的含量,采用以下方案:
硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放.某校兴趣小组欲测定硫酸工业尾气中二氧化硫的含量,采用以下方案:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | SO2的催化氧化反应是吸热反应 | |
| B. | SO2的转化率一定为20% | |
| C. | 导出气体中SO3所占的体积分数为$\frac{2}{9}$ | |
| D. | 单位时间内进人接触室的气体与从接触室导出的气体的物质的量之比为10:9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
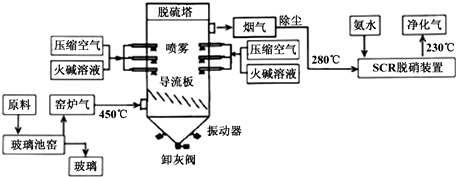
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com