
| A、生石灰 | B、漂白粉 |
| C、明矾 | D、硫酸铁 |
科目:高中化学 来源: 题型:
| A、升温增压 | B、降温增压 |
| C、升温减压 | D、降温减压 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“雪花→水→水蒸气→氧气和氢气”变化中,被破坏的粒子间的作用力依次是:氢键、氢键、极性键 |
| B、晶体CO2和H2O中,化学键类型相同,晶体类型也相同 |
| C、SiO2晶体最小的环上,有6个Si原子和6个O原子 |
| D、金刚石和石墨的熔点都较高,是因为二者都为原子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO |
| B、CO2 |
| C、CO和 CO2 |
| D、C2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硬度很大、熔点很高 |
| B、高温下可分解气化 |
| C、良好的热稳定性 |
| D、较强的还原性,易燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HF═H++F- |
| B、Ba(OH)2═Ba2++2OH- |
| C、H3PO4═3H++PO43- |
| D、NH3?H2O═NH4++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 离子 | Fe3+ | Al3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀的pH | 2.7 | 3.7 | 7.0 | 7.8 | 9.3 |
| 沉淀完全的pH | 3.7 | 4.7 | 9.6 | 9.8 | 10.8 |
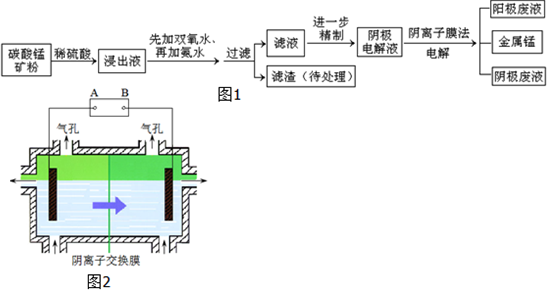
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com