
【题目】有一含Ni的单核六配位配合物,其阳离子空间结构为八面体。1mol该配合物的稀水溶液与足量![]() 混合生成
混合生成![]() 沉淀233g;将溶液过滤,滤液与硝酸银溶液混合不生成沉淀。元素分析表明该配合物所含部分原子个数比为
沉淀233g;将溶液过滤,滤液与硝酸银溶液混合不生成沉淀。元素分析表明该配合物所含部分原子个数比为![]() 。
。
(1)请画出Ni的价电子排布图:______________________,H、N、O的电负性由大到小的顺序为______________________。
(2)滤液与硝酸银溶液混合不生成沉淀的原因是___________________________________。
(3)该配合物阴离子的中心原子杂化方式为____________,请写出该配合物的化学式:________________。
(4)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可以在多个原子间运动,形成“离域![]() 键”。下列微粒中存在“离域
键”。下列微粒中存在“离域![]() 键”的是_________
键”的是_________![]() 填序号
填序号![]() 。
。
A.![]()
![]()
![]()
![]() 苯
苯
(5)如图是六方NiAs晶胞的晶胞图及坐标参数,其中![]() ,
,![]() ,
,![]() 。晶胞顶点、棱上小球为Ni,As在体内。
。晶胞顶点、棱上小球为Ni,As在体内。

①写出As的配位数为_________,Ni的配位数为_________。
②已知晶胞参数为![]() ,
,![]() ,则晶胞的密度为____________
,则晶胞的密度为____________![]() 写表达式
写表达式![]() 。
。
【答案】![]()
![]() 氯与Ni形成配位键不能解离,故不与
氯与Ni形成配位键不能解离,故不与![]() 形成沉淀
形成沉淀 ![]() 杂化
杂化 ![]()
![]()
![]() 6
6 ![]()
【解析】
![]() 的价电子排布式为
的价电子排布式为![]() ,所以排布图为
,所以排布图为![]() ;非金属性越强,电负性越大,所以电负性大小顺序为
;非金属性越强,电负性越大,所以电负性大小顺序为![]() ;
;
![]() 由于配合物中有氯,但是加硝酸银却没有现象,说明氯没有在配合物的外界形成阴离子,所以氯应该是和Ni形成了配位键,所以不与
由于配合物中有氯,但是加硝酸银却没有现象,说明氯没有在配合物的外界形成阴离子,所以氯应该是和Ni形成了配位键,所以不与![]() 形成沉淀;
形成沉淀;
![]() 根据产生硫酸钡沉淀可知阴离子为硫酸根离子,硫酸根离子中硫是
根据产生硫酸钡沉淀可知阴离子为硫酸根离子,硫酸根离子中硫是![]() 杂化;由于配合物为单核六配位配合物,其阳离子空间结构为八面体,元素分析表明该配合物所含部分原子个数比为
杂化;由于配合物为单核六配位配合物,其阳离子空间结构为八面体,元素分析表明该配合物所含部分原子个数比为![]() ,所以有6个配体,一个为氯,其余为
,所以有6个配体,一个为氯,其余为![]() ,其化学式为
,其化学式为![]() ;
;
![]() 中S和苯中的C采取
中S和苯中的C采取![]() 杂化,原子在同一平面,有相互平行的p轨道,则p电子可以在多个原子间运动,形成“离域
杂化,原子在同一平面,有相互平行的p轨道,则p电子可以在多个原子间运动,形成“离域![]() 键”,B和C中
键”,B和C中![]() 和
和![]() 的中心原子都是
的中心原子都是![]() 杂化,原子不在同一平面,不能形成“离域
杂化,原子不在同一平面,不能形成“离域![]() 键”;
键”;
答案选AD;
根据晶胞结构看出As周围最近的Ni有6个;根据化学式NiAs判断两种原子个数比为
![]() ,所以Ni的配位数也为6;一个晶胞有2个NiAs,体积为
,所以Ni的配位数也为6;一个晶胞有2个NiAs,体积为![]() ,所以密度为
,所以密度为![]() 。
。


科目:高中化学 来源: 题型:
【题目】某原子核外电子排布式为1s22s22p3,下列说法正确的是( )
A.该原子的核外电子排布图为![]()
B.该原子核外有3种能量不同的电子
C.该原子核外最外层上有3种运动状态不同的电子
D.该原子核外最外层电子占据3个原子轨道
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前四周期元素A、B、C、D、E原子序数依次增大。已知:A、C同主族,A的原子最外层电子数是次外层的3倍,B的氧化物既能溶于强酸,又能溶于强碱,D的原子半径是第3周期中最小的,E是形成骨骼和牙齿的主要元素,且E单质能和水反应。则下列分析错误的是
A. A的离子结构示意图为![]()
B. D的最高价氧化物的水化物的酸性大于C的最高价氧化物的水化物的酸性
C. E和D形成的离子化合物ED2的电子式为![]()
D. B的氧化物为离子化合物,只含离子键,其晶体为离子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图的实验装置可用于研究SO2转化为SO3的转化率。已知:SO3的熔点是16.8℃,沸点是44.8℃。A处为SO2气体发生装置,C处为SO2与O2反应的装置。
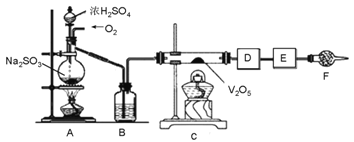
完成下列填空:
(1).A处的化学反应方程式为__________________,仪器F的名称为___________________________。
(2).根据实验需要,应该在D、E处连接合适的装置。请从下图中选择,将所选装置的序号填入相应的空格,D:________________,E:______________。

(3).用amolNa2SO3粉末与足量浓硫酸进行此实验,当A处反应结束时,再继续通入一段时间O2,最后测得E处装置增重bg,则此时SO2的转化率为_____%(用含a、b的代数式表示)。
(4).若Na2SO3变质,会影响到SO2的转化。现欲检验某Na2SO3样品是否变质,你的方法是____________________________________________________________________________________________。
(5).实验结束后,如果将收集了SO3的装置敞口露置于空气中,可看到装置出口处产生大量白雾,其原因是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是![]()
A.![]() 的溶液不一定呈中性
的溶液不一定呈中性
B.除去氯化镁溶液中的氯化铁杂质,可加入碳酸镁调节pH
C.强碱滴定弱酸可选用酚酞作指示剂,滴定终点现象是无色突变为粉色
D.![]() 时,某溶液中由水电离产生的
时,某溶液中由水电离产生的![]() ,该溶液
,该溶液![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NA表示阿伏加德罗常数,下列说法中正确的是( )
A. 53g碳酸钠中含NA个CO32—B. 0.1molOH—含NA电子
C. 1.8g重水(D2O)中含NA个中子D. 标准状况下11.2L臭氧(O3)中含NA个氧原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下有①6.72L甲烷②3.01×1023个氯化氢分子③13.6 g硫化氢④0.2 mol NH3。下列对这四种气体的关系从小到大表示不正确的是
A.体积:④<①<②<③B.密度:①<④<③<②
C.质量:④<①<③<②D.氢原子数:②<④<③<①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据图中氮元素及其化合物的转化关系,回答问题:
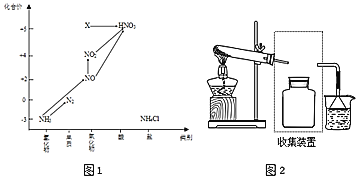
(1)图1中,X的化学式为_____,从化合价上看,X具有______性(“氧化”、“还原”)。
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为__________。
②下列试剂不能用于干燥NH3的是__________(填字母)。
A.浓硫酸 B.碱石灰 C.生石灰
③若要收集一瓶氨气,采用的方法是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 W、X、Y、Z 的原子序数依次增大,W、X 原子的最外层电子数之比为 4:3,Z 原子比 X 原子的核外电子数多 4。下列说法正确的是
A.W、Y、Z 的电负性大小顺序一定是 Z>Y>W
B.W、X、Y、Z 的原子半径大小顺序可能是 W>X>Y>Z
C.Y、Z 形成的分子空间构型可能是正四面体
D.WY2 分子中![]() 键与π键的数目之比是 2:1
键与π键的数目之比是 2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com