

分析 混合物加入水过滤,得到白色沉淀,白色沉淀加入盐酸生成二氧化碳和氯化钡,可知白色沉淀为BaCO3,无色溶液加入硝酸银溶液生成硝酸钾和氯化银,可知无色溶液含有KCl,可知混合物有K2CO3和BaCl2组成,以此解答该题.
解答 解:混合物加入水过滤,得到白色沉淀,白色沉淀加入盐酸生成二氧化碳和氯化钡,可知白色沉淀为BaCO3,无色溶液加入硝酸银溶液生成硝酸钾和氯化银,可知无色溶液含有KCl,可知混合物有K2CO3和BaCl2组成,
(1)有以上分析可知混合物由K2CO3和BaCl2组成,故答案为:K2CO3;BaCl2;
(2)K2CO3和BaCl2在溶液中发生CO32-+Ba2+=BaCO3↓;BaCO3加入盐酸发生反应生成二氧化碳和氯化钡,反应的离子方程式为BaCO3+2H+=Ba2++CO2↑+H2O,KCl与硝酸银溶液生成硝酸钾和氯化银,反应的离子方程式为Ag++Cl-=AgCl↓,
故答案为:CO32-+Ba2+=BaCO3↓;BaCO3+2H+=Ba2++CO2↑+H2O;Ag++Cl-=AgCl↓.
点评 本题属于框图式的推断题,为高频考点和常见题型,侧重于学生的分析能力的考查,在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可,难度不大.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:解答题
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将少量氯化钴晶体溶于一定浓度的盐酸溶液呈紫色,加热后溶液颜色变成蓝色 | |
| B. | 中和热测定实验中,环形玻璃搅拌棒不能用铜质搅拌棒代替 | |
| C. | 容量瓶、分液漏斗、滴定管使用时都必须检查是否漏水 | |
| D. | 滴定管水洗后必须烘干才能使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
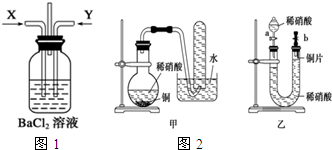 请分析回答某同学在探究浓硫酸、稀硫酸、浓硝酸、稀硝酸分别与铜反应的实验中发生的有关问题.
请分析回答某同学在探究浓硫酸、稀硫酸、浓硝酸、稀硝酸分别与铜反应的实验中发生的有关问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com