
下列关于有机物的叙述正确的是( )
A.甲烷、甲苯、甲醇都可以发生取代反应
B.聚乙烯可发生加成反应
C.淀粉、纤维素、蛋白质、油脂都属于高分子化合物
D.乙醇和乙酸可以用无色的酚酞试液鉴别
科目:高中化学 来源: 题型:
类推的思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才能决定其正确与否,下列几种类推结论中错误的是( )
①钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2 ②氢氧化铝加热能分解为金属氧化物和水;氢氧化镁、氢氧化铁也能加热分解生成金属氧化物和水 ③碳酸钠、碳酸氢钠溶液均显碱性;钠盐溶液均能使酚酞变红 ④钠和硫反应生成Na2S;镁、铝、铁均能与硫直接化合生成相应的硫化物
A.①④ B.①③
C.②④ D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
在真空密闭容器中加入a mol固体PH4I,在一定的温度下发生如下反应:
PH4I(s)PH3(g)+HI(g)①
4PH3(g)P4(g)+6H2(g)②
2HI(g)H2(g)+I2(g)③
以上三个反应建立平衡后,测得HI为b mol,I2为c mol,H2为d mol,求:
(1)平衡后容器内P4和PH3的物质的量:________(用代数式表示)。
(2)a、b、c三者遵循的关系:a>________(填b、c的关系式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组用废铁泥(主要成分为Fe2O3、FeO和少量Fe)制备磁 性Fe3O4纳米材料的流程示意图如下:
性Fe3O4纳米材料的流程示意图如下:

已知:R= ,步骤⑤中,相同条件下测得Fe3O4的产率与R的关系如图所示。
,步骤⑤中,相同条件下测得Fe3O4的产率与R的关系如图所示。

(1)步骤②中,主要反应的离子方程式是__________________。
(2)已知:Fe3+在pH=2.8时沉淀完全;Fe2+在pH=6.3时开始沉淀,在pH=8.3时沉淀完全。
步骤③中,用NaOH溶液调pH至9,原因是_________________。
(3)浊液D中铁元素以FeOOH形式存在。步骤④中,反应的化学方程式是_________________________________________________。
(4)下列说法正确的是________(填选项字母)。
a.步骤④中,当反应完成后需再加热一段时间
b.步骤⑤中,反应过程中需要不断补充碱液
c.步骤⑤恰好反应时, =2:1
=2:1
d.当 =
= 时,Fe3O4的产率最高
时,Fe3O4的产率最高
查看答案和解析>>
科目:高中化学 来源: 题型:
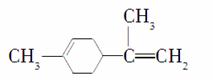 (2014·武汉市调研)柠檬烯是一种食用香料,其结构简式如图,有关柠檬烯的分析正确的是( )
(2014·武汉市调研)柠檬烯是一种食用香料,其结构简式如图,有关柠檬烯的分析正确的是( )
A.柠檬烯的一氯代物有7种
B.柠檬烯和丁基苯互为同分异构体
C.柠檬烯的分子中所有的碳原子可能在同一个平面上
D.在一定条件下,柠檬烯可以发生加成、取代、氧化、还原等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:


实验步骤:
在A中加入4.4 g的异戊醇,6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50 min,反应液冷至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。回答下列问题:
(1)仪器B的名称是________________。
(2)在洗涤操作中,第一次水洗的主要目的是________________; 第二次水洗的主要目的是______________________。
(3)在洗涤、分 液操作中,应充分振荡,然后静置,待分层后________(填选项字母)。
液操作中,应充分振荡,然后静置,待分层后________(填选项字母)。
a.直接将乙酸异戊酯从分液漏斗上口倒出
b.直接将乙酸异戊酯从分液漏斗下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是_________________________。
(5)实验中加入少量无水MgSO4 的目的是____________________。
的目的是____________________。
(6)在蒸馏操作中,仪器选择及安装都正确的是_______ _(填选项字母)。
_(填选项字母)。

(7)本实验的产率是________(填选项字母)
A.30% B.40% C.60% D.90%
(8)在进行蒸馏操作时,若从130 ℃开始收集馏分,会使实验的产率偏________(填“高”或 “低”),其原因是
“低”),其原因是
__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在2Na2O2+2H2O=4NaOH+O2↑中下列说法正确的是 ( )
A.每生成224mLO2,转移0.01mol e-
B.过氧化钠的摩尔质量为78g
C. 将0.01mol Na2O2加入到水中得到100mL溶液,溶质物质的量浓度为0.2mol/L
D.在Na2O2中阴阳离子个数比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH 、Cl-、Mg2+、Ba2+、CO
、Cl-、Mg2+、Ba2+、CO 、SO
、SO ,现取三份100 mL溶液进行如下实验:
,现取三份100 mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生。
(2)第二份加足量NaOH溶液加热后,收集到气体0.04 mol。
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。
根据上述实验,以下推测正确的是( )
A.K+不一定存在
B.100 mL溶液中含0.01 mol CO
C.Cl-可能存在
D.Ba2+一定不存在,Mg2+可能存在
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com