
 ��
��
 $\stackrel{һ������}{��}$
$\stackrel{һ������}{��}$
 ��Ӧ�Ļ�ѧ����ʽ��
��Ӧ�Ļ�ѧ����ʽ��
���� ��1�����ݷ�������Ԫ�غ���Ԫ��������Ϊ35.5��16��������ԭ�Ӻ���ԭ�Ӹ�����ȣ�����Է�������Ϊ156.5�������к��б���֪����1����ԭ�Ӻ�1����ԭ�ӣ�
��2���÷����к��б������ĸ�ȡ������������ͬ�ļ����ڼ�λ���ǻ�����ԭ�Ӵ��ڶ�λ����������������1molPCMX����2molBr2��Ӧ������������λ�ڷ��ǻ��ļ�λ��
��3������������PCMX���ϵ���ԭ������������ȡ����Ӧ����һ�ȴ��
��4������������Ϣ���⣻
��5��PCMX��ͬ���칹���У�����ȡ�������ܸ��Ȼ���������ɫ��Ӧ���ǻ�ֱ�����ڱ����ϣ����������һ��������������-CH2-CH2-Cl��-CHCl-CH3���ڱ����ϸ����ڼ�����֣�
��� �⣺��1�����ݷ�������Ԫ�غ���Ԫ��������Ϊ35.5��16��������ԭ�Ӻ���ԭ�Ӹ�����ȣ�����Է�������Ϊ156.5�������к��б���֪����1����ԭ�Ӻ�1����ԭ�ӣ�$\frac{156.5-35.5-16}{12}$=8.75�����Է���ʽΪC8H9ClO���ʴ�Ϊ��C8H9ClO��
��2���÷����к��б������ĸ�ȡ������������ͬ�ļ����ڼ�λ���ǻ�����ԭ�Ӵ��ڶ�λ����������������1molPCMX����2molBr2��Ӧ������������λ�ڷ��ǻ��ļ�λ����PCMX�Ľṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��3������������PCMX���ϵ���ԭ������������ȡ����Ӧ����һ�ȴ����ѧ����ʽ�� ��
��
�ʴ�Ϊ�� ��
��
��4��PCMX�� ��Ӧ�Ļ�ѧ����ʽ��
��Ӧ�Ļ�ѧ����ʽ�� ��
��
�ʴ�Ϊ�� ��
��
��5������ͬ���칹���У�����ȡ�������ܸ��Ȼ���������ɫ��Ӧ���ǻ�ֱ�����ڱ����ϣ����������һ��������������-CH2-CH2-Cl��-CHCl-CH3���ڱ����ϸ����ڼ�����֣� ����6�֣�
����6�֣�
�ʴ�Ϊ��6��
���� ���⿼���л�������ʺ�ͬ���칹�����д����Ŀ�ѶȲ�����ע����ճ����л���Ĺ����ŵ����ʣ���ס��Ӧ�����������л��ﷴӦ�Ļ�ѧ����ʽҪ��д��


 ������ĩ��ϰ��ѵ��ϵ�д�
������ĩ��ϰ��ѵ��ϵ�д� С��ʿ��ĩ����100��ϵ�д�
С��ʿ��ĩ����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeCl3 | B�� | Cl2 | C�� | KClO3 | D�� | HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
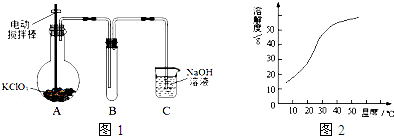
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 +CH3COCHCOOC2H5$��_{10�����12h}^{ŨH_{2}SO_{4}}$
+CH3COCHCOOC2H5$��_{10�����12h}^{ŨH_{2}SO_{4}}$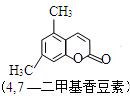

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe3+ SCN-Na+ NO${\;}_{3}^{-}$ | B�� | Cu2+ SO${\;}_{4}^{2-}$HCO${\;}_{3}^{-}$K+ | ||
| C�� | CO${\;}_{3}^{2-}$Na+Cl-K+ | D�� | Ba2+ Ca2+ Cl-NO${\;}_{3}^{-}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��10-4 | B�� | 55.6��107 | C�� | 1��107 | D�� | 6.02��1021 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com