
【题目】下列物质中:①NaCl;②NaOH;③NH3·H2O;④CH3COOH溶液;⑤BaSO4;⑥H2O;⑦HCl;⑧H2SO4;⑨CO2;⑩酒精溶液(均填写编号回答)
(1)pH相等的②的溶液和③的溶液等体积加水稀释相同倍数后,pH大的是______.
(2)有pH均为2的④、⑦、⑧三种物质的溶液,物质的量浓度大到小的顺序为______,若分别用这三种酸中和含等物质的量NaOH的溶液,所需酸溶液的体积分别为a、b、c,则a、b、c的大小关系是__________.
(3)某温度时,1mol·L-1的醋酸溶液电离平衡常数为1.0×10-8,达平衡时,溶液中氢离子浓度是______________.
【答案】 ③ ④>⑦>⑧ b=c>a 1.0×10-4mol·L-1
【解析】(1)一水合氨是弱电解质,在水溶液中存在电离平衡,加水稀释时,氢氧根离子物质的量增大,NaOH是强电解质,加水稀释时氢氧根离子物质的量不变,加水稀释相同倍数后,一水合氨溶液中氢氧根离子物质的量浓度大,pH大,故答案为③;(2)醋酸是一元弱酸,盐酸是一元强酸,硫酸是二元强酸,pH相同时,醋酸浓度大于盐酸,盐酸浓度大于硫酸;pH相同时,氢离子浓度相同,醋酸不完全电离,醋酸浓度远远大于盐酸和硫酸,若分别用pH相等的这三种酸中和含等物质的量NaOH的溶液,所需酸溶液的体积醋酸<盐酸=硫酸,故答案为:④>⑦>⑧;b=c>a;(3)醋酸的电离方程式为:CH3COOHH++CH3COO-,其平衡常数表达式为K=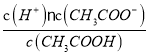 ;c2(H+)=Kc(CH3COOH) =1.0×10-8×1mol/L=1.0×10-8mol/L,c(H+)=1.0×10-4mol/L。
;c2(H+)=Kc(CH3COOH) =1.0×10-8×1mol/L=1.0×10-8mol/L,c(H+)=1.0×10-4mol/L。


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:
【题目】根据下列各图曲线表征的信息,得出的结论不正确的是


A. 图1表示常温下向体积为10 mL 0.1 mol·L-1NaOH溶液中逐滴加入0.1 mol·L-1CH3COOH溶液后溶液的pH变化曲线,则b点处有:c(CH3COOH)+c(H+)=c(OH-)
B. 图2表示用水稀释pH相同的盐酸和醋酸时溶液的pH变化曲线,其中Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a
C. 图3表示H2与O2发生反应过程中的能量变化,H2的燃烧热为285.8 kJ·mol-1
D. 由图4得出若除去CuSO4溶液中的Fe3+,可采用向溶液中加入适量CuO,调节溶液的pH至4左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.金属钠和水反应:Na+2H2O=Na++2OH-+H2↑
B.大理石与稀硝酸反应:CaCO3+2H+=Ca2++CO2↑+H2O
C.硫酸溶液与氧氧化钡溶液混合:H++SO42-+Ba2++OH-=H2O+BaSO4↓
D.MgC12溶液与过量氨水反应:Mg2++2OH-=Mg(OH)2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化锆(ZrO2)是最重要的氧离子固体电解质,用于制造燃料电池、氧气含量测定仪等。可由锆英砂(主要成分为ZrSiO4,也可表示为ZrO2·SiO2;含有少量Fe2O3、Al2O3、SiO2杂质)通过如工艺流程法制得。
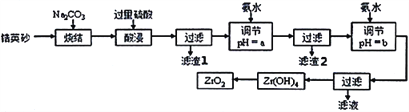
已知:①ZrO2具有两性,高温与纯碱共熔生成可溶于水的Na2ZrO3,与酸反应生成ZrO2+。
②部分金属离子在实验条件下开始沉淀和完全沉淀的pH如下表。
金属离子 | Fe3+ | Al3+ | ZrO2+ |
开始沉淀时pH | 1.9 | 3.3 | 6.2 |
沉淀完全时pH | 3.2 | 5.2 | 8.0 |
请回答下列问题:
(1)已知Zr元素的原子序数是40,请写出它在周期表中的位置:____________________________。
(2)烧结时ZrSiO4发生反应的化学方程式为__________________________;滤渣1的化学式为__________。
(3)调节pH=a时,a的范围应该是__________________;用氨水调节pH=b时,所发生反应的离子方程式为_______________________________________。
(4)本题的流程中,一共有三步过滤操作,北中最后一步过滤所得的Zr(OH)4沉淀需要洗涤,证明该沉淀已经洗涤干净的最佳操作方法是:______________________________________。
(5)工业上用铝热法冶炼锆,写出以ZrO2通过铝热法制取锆的化学方程式:________________。
(6)一种新型燃料电池用掺杂Y2O3的ZrO2晶体作电解质在熔融状态下传导O2-,一极通入空气,另一极通入乙烷,写出负极的电极反应式:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表前四周期的一部分,下列对相关元素的叙述正确的是( )
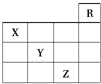
①X元素的原子有二个电子层,处于周期表的第15个纵行;②Z的原子序数为31,单质常温下为液体;③气态氢化物水溶液的酸性 X<Y<Z;④X的气态氢化物与Y的最高价氧化物的水化物能反应生成盐;⑤Z的原子序数比Y大19,Y的原子序数比X大 9。
A. 只有② B. 只有①③④⑤ C. 只有①②③④ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的位置如图所示。下列说法中正确的是

A. W的最高价氧化物对应的水化物是强酸
B. Y的原子半径在同周期主族元素中最大
C. W的非金属性比Z的弱
D. Z的气态氢化物的稳定性在同主族元素中最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用15N可以测定亚硝酸盐对地下水质的污染情况。
(1)下列说法正确的是______。
A.14N与15N为同种核素 B.14N的第一电离能小于14C
C.15NH3与14NH3均能形成分子间氢键 D.14CH315NH2与CH3CH2NH2互为同系物
(2)15N的价层电子排布图为_______,15NH4Cl的晶胞与CsCl相同,则15NH4Cl晶体中15NH4+的配位数为_____;15NH4+中15N的杂化轨道类型为_________。
(3)工业上电解法处理亚硝酸盐的模拟工艺如图:
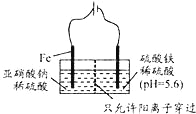
已知:阳极区发生化学反应:2N02+8H++6Fe2+═N2↑+6Fe3++4H2O
①阳极电极反应方程式是______(不考虑后续反应);
②若硫酸溶液浓度过大,阴极区会有气体逸出,该气体为________(填化学式); 该现象表明c(H+)越大,H+氧化性越_______;
③若电解时电路中有0.6mol电子转移,且NaNO2有剩余,则电解池中生成________molNa2SO4。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能在溶液中大量共存的一组离子是
A. NH4+、Ag+、PO43-、Cl- B. Fe3+、H+、I-、 HCO3-
C. K+、 Na+、 NO3-、 MnO4- D. Al3+、Mg2+、SO42-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将固体NH4I置于密闭容器中,在一定温度下发生下列反应:①NH4I(s)![]() NH3(g)+HI(g);②2HI(g)
NH3(g)+HI(g);②2HI(g)![]() H2(g)+I2(g) 达到平衡时,c(H2)=0.7 mol·L-1,c(HI)=4 mol·L-1,则此温度下反应①的平衡常数为
H2(g)+I2(g) 达到平衡时,c(H2)=0.7 mol·L-1,c(HI)=4 mol·L-1,则此温度下反应①的平衡常数为
A. 2.8 B. 18.8 C. 21.6 D. 29.16
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com