
| A. | ①②③ | B. | ④⑤⑥ | C. | ④⑥ | D. | ②④⑥ |
分析 ①碳酸根离子为多元弱酸根离子,分步水解,以第一步为主;
②铵根离子水解生成一水合氨和氢离子;
③水解可逆过程,应使用可逆号;
④铜离子水解生成氢氧化铜和氢离子;
⑤碳酸氢根离子水解生成碳酸和氢氧根离子;
⑥亚硫酸根离子水解生成亚硫酸氢根离子和氢氧根离子.
解答 解:①碳酸根离子为多元弱酸根离子,分步水解,以第一步为主,水解方程式:CO32-+H2O?$\stackrel{.}{?}$HCO3-+OH-
,故错误;
②铵根离子水解生成一水合氨和氢离子,水解的离子方程式:NH4++H2O$\stackrel{.}{?}$?NH3•H2O+H+,故错误;
③氟化钠中氟离子水解生成氢氟酸和氢氧根离子,离子方程式:F-+H2O$\stackrel{.}{?}$HF+OH-,故错误;
④铜离子水解生成氢氧化铜和氢离子,离子方程式:Cu2++2H2O$\stackrel{.}{?}$?Cu(OH)2+2H+,故正确;
⑤碳酸氢根离子水解生成碳酸和氢氧根离子,离子方程式:HCO3-+H2O?$\stackrel{.}{?}$OH-+H2CO3,故错误;
⑥亚硫酸根离子水解生成亚硫酸氢根离子和氢氧根离子,离子方程式:SO32-+H2O?HSO3-+OH-,故正确;
故选:C.
点评 本题考查了盐类水解的离子方程式,明确盐类水解的规律是解题关键,注意单离子水解为可逆过程,应使用可逆符号,题目难度不大.


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:填空题
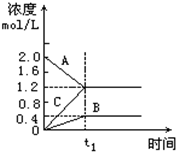 如图表示800℃时A、B、C三种气体物质的浓度随时间的变化情况,t1是到达平衡状态的时间,t1为2分钟.试回答:
如图表示800℃时A、B、C三种气体物质的浓度随时间的变化情况,t1是到达平衡状态的时间,t1为2分钟.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Ba2+、NO3-、Cl- | B. | H+、Mg2+、Na+、SO42- | ||
| C. | CO32-、K+、Cl-、Na+ | D. | Fe2+、NO3-、SO42-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ①②③④ | D. | ①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 充电时铁做负极,NiO2做正极 | |
| B. | 放电时阴极上的电极反应为:Fe(OH)2+2e-=Fe+2OH- | |
| C. | 放电时,电解质溶液中的阴离子是向正极方向移动 | |
| D. | 蓄电池的两个电极必须浸入在碱性溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 分子式为C26H28O6N | |
| B. | 遇FeCl3溶液不能发生显色反应 | |
| C. | 1mol该物质最多能与8mol氢气发生加成反应 | |
| D. | 1mol该物质最多能与4molNaOH溶液完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com