
 乙基香兰素是当今世界上最重要的合成香料之一,是食品添加剂中不可缺少的重要原料,其结构简式如图所示.
乙基香兰素是当今世界上最重要的合成香料之一,是食品添加剂中不可缺少的重要原料,其结构简式如图所示. 、
、 ;
; .
.
 .
. .
. .
. 分析 (1)根据乙基香兰素含有的官能团和苯环的结构特点判断可能具有的性质;
(2)M可与饱和溴水反应生成白色沉淀,说明苯环上含有-0H,N的质谱图显示相对分子质量为32,红外光谱图上发现有O-H键、C-H键和C-O键的振动吸收,则N为CH3OH,则X应为羟基苯乙酸甲酯,两种取代基有邻、间、对位置;
(3)乙基香兰素的另一种同分异构体Y,分子中苯环上只有1个取代基,它可以和碳酸氢钠反应生成CO2,说明含有-COOH,
A能发生银镜反应,说明A中含有-CHO,则Y中应含有-CH2OH,则Y为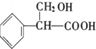 ,B为
,B为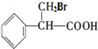 ,
,
C能发生加成反应,由B消去反应生成,结构式为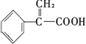 ,以此解答该题.
,以此解答该题.
解答 解:(1)A.该物质含有酚羟基,能氯化铁反应,不与氯化亚铁反应,故A错误;
B.乙基香兰素的分子式应为C9H10O3,而香兰素的分子式应为C7H6O3,故B错误;
C.乙基香兰素含有酚羟基,容易被氧气氧化,所以应密封保存,故C正确;
D.根据苯环中所有原子共面,碳氧双键中所有原子共面,单键可以旋转的特点,可知该分子内最多有18个原子共面,故D正确,
故答案为:AB;
(2)M可与饱和溴水反应生成白色沉淀,说明苯环上含有-0H,N的质谱图显示相对分子质量为32,红外光谱图上发现有O-H键、C-H键和C-O键的振动吸收,则N为CH3OH,X和乙基香兰素互为同分异构体,分子式为C9H10O3,则X应为羟基苯乙酸甲酯,两种取代基有邻、间、对位置,结构为 、
、 、
、 ,
,
故答案为: ;
; ;
; (其中任意两个);
(其中任意两个);
(3)①乙基香兰素的另一种同分异构体Y,分子中苯环上只有1个取代基,它可以和碳酸氢钠反应生成CO2,说明含有-COOH,
A能发生银镜反应,说明A中含有-CHO,则Y中应含有-CH2OH,则Y为 ,分子中含有羧基和羟基,
,分子中含有羧基和羟基,
故答案为:羟基、羧基;
②Y为 ,B为
,B为 ,发生的为取代反应,
,发生的为取代反应,
故答案为:取代反应;
③A为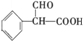 ,含有-CHO,与氢氧化铜在加热条件下发生:
,含有-CHO,与氢氧化铜在加热条件下发生: ,
,
故答案为: ;
;
④B为 ,C结构式为
,C结构式为 ,B发生消去反应生成C,
,B发生消去反应生成C,
反应的化学方程式为 ,
,
故答案为: ;
;
⑤Y为 ,分子中含有-OH、-COOH,能发生缩聚反应生成
,分子中含有-OH、-COOH,能发生缩聚反应生成 ,
,
故答案为: .
.
点评 本题考查有机物的结构和性质,题目难度中等,本题注意把握有机物的官能团的结构和性质,为解答该题题目的关键,注意同分异构体的判断.


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同样是在氯气中点燃,铁少量生成的是氯化铁,过量时则生成氯化亚铁 | |
| B. | 同样是试纸检测,检验气体需要润湿,检验溶液时则一般不能润湿 | |
| C. | 同样是配制溶液,一定质量分数的溶液配制使用烧杯,而一定物质的量浓度的溶液配制则还需要容量瓶 | |
| D. | 同样是浓溶液(设其质量分数为ω )与水等体积混合,所得硫酸的浓度大于 0.5ω,氨水的则小于 0.5ω |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | C-H | H-H | C-O | C=O | H-O |
| 键能/kj•mol-1 | a | b | c | d | e |
| HA | H2B | HC | ||
| Ka | Ka1 | Ka2 | Ka3 | Ka4 |
| 数值 | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+、HCO3-、Cl-、K+ | B. | OH-、CO32-、Cl-、K+ | ||
| C. | Ba2+、Na+、OH-、NO3- | D. | Cu2+、NO3-、OH-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠和盐酸溶于水都发生电离,克服粒子间作用力的类型相同 | |
| B. | 氯化铵和水玻璃都属于离子化合物 | |
| C. | 直径介于1nm-10nm之间的微粒称为胶体 | |
| D. | 由IA族和VIA族元素可以形成含有原子个数比为l:1,离子个数比为2:l的离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胃舒平中含有氢氧化铝,可治疗胃酸过多:Al(OH)3+3HCl═AlCl3+3H2O | |
| B. | 碳铵是一种常用化肥,60℃分解完全:2NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O↑ | |
| C. | 生石灰可用作建筑材料:CaO+H2O=Ca(OH)2,属于化合反应 | |
| D. | 实验室常用氧化还原反应制备氧气:2H2O2 $\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据醋酸溶液中分子和离子共存,即可证明溶液达到了电离平衡状态 | |
| B. | c(CH3COO-)=c(H+),则醋酸溶液达到电离平衡状态 | |
| C. | 当NH3•H2O达到电离平衡时,溶液中NH3•H2O和OH-的浓度肯定相等 | |
| D. | 磷酸是分步电离的,电离程度依次减弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com