
| A.①⑤ | B.③④⑤ | C.①②③⑤ | D.①②③④⑤ |
科目:高中化学 来源:不详 题型:实验题
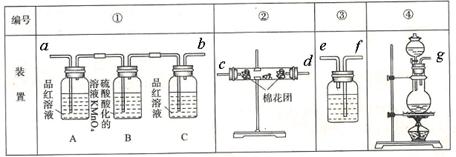
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
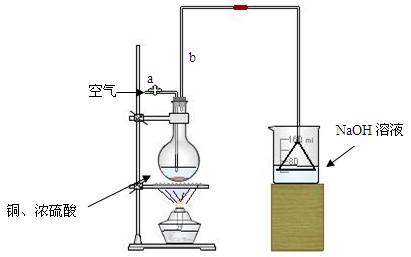
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 现象或反应 | 原理解释 I |
| A | 铝箔在酒精灯 火焰上加热熔化但不滴落 火焰上加热熔化但不滴落 | 铝箔表面生成的氧化物炅有高熔点 |
| B | 钠和氧气在加热条件下进行反应 | 该反应为吸热反应 |
| C | 碳酸钠和氢氧化钠溶液中滴加酚酞,溶液都呈红色 | 碳酸钠和氢氧化钠都玷碱 |
| D | 将CH3CH2Br与NaOH溶液混合加热,再滴加AgNO3溶液,未产生浅黄色沉淀 | CH3CH2Br未发生水鮮 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
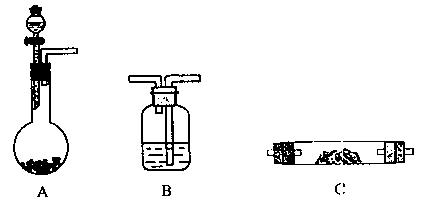
| 选用的仪器(填字母) | 加入的试剂 |
| A | 稀盐酸、大理石 |
| | |
| | |
| | |
| | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

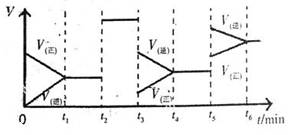
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com