
| A. | 紫色石蕊试液 | B. | 氯化钡溶液 | ||
| C. | 酸性高锰酸钾溶液 | D. | 澄清石灰水 |
分析 SO2与CO2都是酸性氧化物,SO2和CO2气体都可使澄清石灰水变浑浊,SO2具有还原性和漂白性,以此解答该题.
解答 解:A.SO2与CO2都是酸性氧化物,与水反应生成碳酸和亚硫酸,SO2和CO2气体都可使紫色石蕊试液变红,不能鉴别,故A错误;
B.盐酸的酸性大于亚硫酸、碳酸,则二者与氯化钡均不反应,现象相同,不能鉴别,故B错误;
C.二氧化碳与高锰酸钾不反应,二氧化硫具有还原性,与高锰酸钾发生氧化还原反应使其褪色,现象不同,可鉴别,故C正确;
D.SO2与CO2都是酸性氧化物,SO2和CO2气体都可使澄清石灰水变浑浊,不能鉴别,故D错误;
故选C.
点评 本题考查物质的鉴别,为高频考点,把握物质的化学性质是解答本题的关键,注意利用反应中不同的现象来鉴别物质,题目难度不大.


 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 随着反应的进行,CO32-在不断消耗 | |
| B. | 该电池的正极的反应式为:4OH-+4e-=O2+2H2O | |
| C. | 放电时CO32-向正极移动 | |
| D. | 该电池负极的反应为:H2+CO32--2e-=H2O+CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
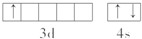 .该元素的原子序数为21,该元素的元素符号是Sc,形成的单质为金属晶体.
.该元素的原子序数为21,该元素的元素符号是Sc,形成的单质为金属晶体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸可做为H2、NH3等气体的干燥剂 | |
| B. | 胆矾遇浓硫酸变白是因为浓硫酸的脱水性 | |
| C. | 足量的锌与一定量的浓硫酸反应会生成氢气 | |
| D. | 可用铝罐储运热的浓硫酸、浓硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水结成冰体积膨胀,密度变小 | |
| B. | CH4、SiH4、GeH4、SnH4的熔点随相对分子质量增大而升高 | |
| C. | He、Ne、Ar、Kr、Xe在水中的溶解度逐渐增大 | |
| D. | 水加热到很高的温度都难以分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com