
��400mL��0.5mol��L-1NaOH��Һ�ͨ��H2S����ַ�Ӧ��������ҺС���������ò����ᾧˮ��ɫ����yg��ͨ��H2SΪxmol����xȡֵ��ͬ���������м��������
��1����Ӧ����ʽΪ________��y=________��
��2����0<x<0.1ʱ����ɫ����Ϊ________��y=________��
��3����x=0.1ʱ����ɫ����Ϊ________��y________��
��4����0.1<x<0.2ʱ����ɫ����Ϊ________��y________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
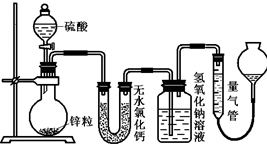 ��ͬŨ�ȵ�������п��Ӧʱ��������Ա���ԭΪSO2��Ҳ�ɱ���ԭΪ������Ϊ����֤��һ��ʵ��ijͬѧ������ͼװ�ý���ʵ�飨ʵ��ʱѹǿΪ10lkPa���¶�Ϊ0�棬п�����ԭ������Ϊ65����
��ͬŨ�ȵ�������п��Ӧʱ��������Ա���ԭΪSO2��Ҳ�ɱ���ԭΪ������Ϊ����֤��һ��ʵ��ijͬѧ������ͼװ�ý���ʵ�飨ʵ��ʱѹǿΪ10lkPa���¶�Ϊ0�棬п�����ԭ������Ϊ65����| n(H2) |
| n(SO2) |
| 64CV-2m |
| m |
| 64CV-2m |
| m |
| n(H2) |
| n(SO2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶ȣ��棩 | 10 | 20 | 30 | 40 | 70 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 |
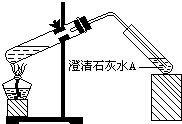
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ijʵ����Ҫ0.5 mol/L�����������FҺԼ400mL��������Һ���ƵĹ��̣��ش��������⣺
��1��ʵ�������Ҫ������ƽ�������룩��ҩ�Ͳ������⣬����Ҫ���������������� ��
��2�����ݼ����֪������Ҫ�������ƹ���������� g��
��3��������Һ�Ĺ����У����²�����ȷ���� ������ţ���
A.���������ƹ������ֽƬ�ϳ���
B.���ձ����ܽ��������ƹ����У���������Һ��������ƿ��
C.���ܽ��������ƹ�����ձ�������ˮϴ��2~3�Σ�����ϴ��Һת�Ƶ�����ƿ��
D.����ƿδ�������ʹ��
E.ҡ�Ⱥ���Һ����ڿ̶��ߣ��ý�ͷ�ιܲ�������ˮ���̶��ߡ�
F.��ˮ��Һ��ӽ��̶���1��2 cm �������ý�ͷ�ιܼ�ˮ��ʹ��Һ�İ�Һ��ǡ����̶�������
��4����ʵ���У�ת��ʱ������Һ��������Ĵ�ʩΪ:
��5����û�н���C�IJ�������������ҺŨ���к�Ӱ�죿_________(�ƫ����ƫС������Ӱ�족)��
��6���������ڸ�ʵ���е������У� �� ��
��7��ȡ0.5 mol/L��NaOH��Һ100 mL��������Na+����ĿΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ijѧ����Ҫ���ռ��������0.5 mol��L-1��NaOH��Һ400mL��
ʵ�����ṩ������������100mL�ձ� ��100 mL��Ͳ ��1000 mL����ƿ ��500 mL����ƿ �ݲ����� ��������ƽ�������룩��
��ش��������⣺
��1������������Ҫ��ȡNaOH���� g��
��2������ʱ������ʹ�õ�������__________ __������ţ���
��ȱ�ٵIJ��������� ���������������ƣ�
��3������ʱ������ȷ�IJ���˳���ǣ���ĸ��ʾ��ÿ������ֻ��һ�Σ�__ ______��
A��������ˮϴ���ձ�2��3�Σ�ϴ��Һ��ע������ƿ����
B����ʢ��NaOH������ձ��м�������ˮ�ܽ�
C�����ձ�������ȴ����Һ�ز�����ע������ƿ��
D��������ƿ�ǽ����������µߵ���ҡ��
E�����ý�ͷ�ιܼ�ˮ��ʹ��Һ����ǡ����̶�����
F������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶�1��2cm��
��4��ʵ�������õ��������������÷ֱ��ǣ� ________ ��________��
��5��������������������н�����������ҺŨ��ƫ�ߵ��� ���������б�ţ�
������ƿʵ��ǰ������ˮϴ�ɾ�����δ���
�ڶ��ݹ۲�Һ��ʱ����
�����ƹ�������©�ˣ�3���в���A
�ܼ�����ˮʱ���������˿̶�
����Һǰû����ȴ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��0112 �¿��� ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com