
����Ŀ��ʹ���Թؽڲ��ķ����������������йء������£��������ƣ� NaUr��������Һ���ã�ȡ�ϲ���Һ�μ����ᣬ��Һ�������Ũ��c��HUr����pH�Ĺ�ϵ��ͼ��ʾ����֪Ksp��NaUr��=4.9��10-5 mol2��L-2��Ka��HUr��=2.0��10-6 mol��L-1������˵����ȷ����

A.�ϲ���Һ�У�c��![]() ��= 7.0��10-2 mol��L-1
��= 7.0��10-2 mol��L-1
B.M��N�ı仯�����У�c(Na+)��c(Ur-)��ֵ����С
C.��c(HUr)=c(Ur-)ʱ��c(Cl-)��c(Ur-)
D.��pH=7ʱ��2c(Na+)��c(Ur-)+c(Cl-)
���𰸡�C
��������
A������Ksp=c(Na+)��c(Ur-)=4.9![]() 10-5�����c(Ur-)=
10-5�����c(Ur-)=![]() ��A����
��A����
B����M��N�ı仯�����У��¶Ȳ��䣬Ksp���䣬��c(Na+)��c(Ur-)��ֵ���䣬B����
C����c(HUr)=c(Ur-)ʱ������Ka(HUr)=2.0![]() 10-6�������pH=5.7����Һ�����ԣ�c(H+)��c(OH-)������NaUr+HCl=NaCl+HUr����֪NaClŨ�ȵ�������Ũ�ȣ���������ҺΪNaCl��HCl��HUr��HUrΪ���ᣬ��c(Ur-)��c(Cl-)��C��ȷ��
10-6�������pH=5.7����Һ�����ԣ�c(H+)��c(OH-)������NaUr+HCl=NaCl+HUr����֪NaClŨ�ȵ�������Ũ�ȣ���������ҺΪNaCl��HCl��HUr��HUrΪ���ᣬ��c(Ur-)��c(Cl-)��C��ȷ��
D�����ݵ���غ㣬c(Na+)+c(H+)=c(Ur-)+c(Cl-)+c(OH-)����pH=7ʱ��c(H+)=c(OH-)������c(Na+)=c(Ur-)+c(Cl-)��D����
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȩ(HCHO)�׳���ȩ,��һ����Ҫ���л�ԭ�ϡ�
I.���ü״�(CH3OH)�Ʊ���ȩ
���ⷨ:CH3OH(g)=HCHO(g)+H2(g) ��H1 = +92.09kJ/mol
������:CH3OH(g) +1/2O2(g)=HCHO(g)+H2O(g) ��H2
(1)��֪:2H2(g)+O2(g)=2H2O(g) ��H3=-483.64 kJ/mol�����H2=_______��
(2)�����ⷨ���,������������ѧ�����ƽϴ���ԭ��Ϊ_______________��
(3)ͼ1Ϊ�״��Ʊ���ȩ��Ӧ��lg K(KΪƽ�ⳣ��)���¶�(T)�ı仯���ߡ�����____(�a����b��)��Ӧ���ⷨ,�ж�����Ϊ_________________��

II.��ȩ����;
(4)����ȩˮ��Һ�백ˮ����������Ƶ�������Ʒ(�ṹ��ʽ��ͼ2)����������ҽҩ�ȹ�ҵ���й㷺��;����ԭ����ȫ��Ӧ����������Ʒ,���ȩ�백�����ʵ���֮��Ϊ_______��
(5)����ȩˮ��Һ��������(NiSO4)��ϣ������ڻ�ѧ����������Ӧ��������CO2��������÷�Ӧ�����ӷ���ʽΪ____________________��
��.��ȩ�ļ��
(6)���ڼ�ȩ�����Σ�����彡����ͨ�����������Լ������м�ȩ�ĺ�����һ��ȼ�ϵ���ͼ�ȩ���崫������ԭ����ͼ3��ʾ����b���ĵ缫��ӦʽΪ_________������·��ת��4��10-4 mol����ʱ���������ڲμӷ�Ӧ��HCHOΪ_______mg��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�̫����ȼ������ʾ��������������أ�̫����ȼ�ϵ�����������ʾ�����£�
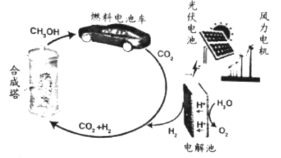
(1)ͼ������ת����ʽ�У��������ܵ��У���������е�������ܡ�___________��(��һ��)��
(2)�ں��º����ܱ������н��еĺϳɷ�ӦΪCO2(g)+ 3H2(g)![]() CH3OH(g)+ H2O(g)��
CH3OH(g)+ H2O(g)��
�ٸ÷�Ӧ����Cu/ZnO����������ҵ���ɻ�ͭ��(CuFeS2)��ұͭʱ�������ಽ��Ӧ������Cu2S��Cu2O�ڸ���������Cu���ų���ʹƷ����Һ��ɫ�����壬д���ò���Ӧ�Ļ�ѧ����ʽ��_________��
����˵����Ӧ�Ѵﵽ��ѧƽ��״̬����_____(����)��
A.��������c(CH3OH)�� c(H2O)=1��1 B.����CO2������������H2O�����
C.���������ܶȲ�����ʱ��仯 D.���������CH3OH���������������ʱ����仯
��������������ʼʱ����1molCO2��3mol H2 �����t1 minʱ������n(H2)= n(H2O)����ʱ������������CH3OH�����ʵ���Ϊ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�ظ�(Cr)����Ȼ����Ҫ��+3�ۺ�+6�۴��ڡ���ش��������⣺
(1)���ø�����(FeOCr2O3)ұ����ȡ�������Ĺ���������ͼ��ʾ��
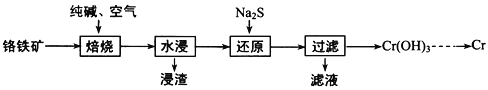
��Ϊ�ӿ챺�����ʺ����ԭ�ϵ������ʣ��ɲ�ȡ�Ĵ�ʩ֮һ��__________________ ��
����ˮ����Ҫ��ý���Һ�IJ�����_________������Һ����Ҫ�ɷ�ΪNa2CrO4��������Һ���м����ữ���Ȼ�����Һ�а�ɫ�������ɣ��� ����ԭ�������з�����Ӧ�����ӷ���ʽΪ___________________________________________________��
(2)��֪ Cr3+��ȫ����ʱ��ҺpHΪ5��(Cr3+Ũ�Ƚ���10-5molL-1����Ϊ��ȫ����)��Cr(OH)3���ܶȻ����� Ksp��_______________��
(3)��ʯī�缫��������(Na2CrO4)��Һ�������ظ�����(Na2Cr2O7)��ʵ��װ����ͼ��ʾ(��֪��2CrO42-+2H+![]() Cr2O72-+ H2O)��
Cr2O72-+ H2O)��
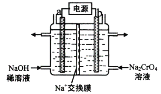
�ٵ缫b���ӵ�Դ��______��(����������������) �� b �������ĵ缫��Ӧ��______________��
�ڵ��һ��ʱ������������Һ��Na+���ʵ�����a mol��Ϊb mol���������������ظ����Ƶ����ʵ�����_______________mol ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I�������г��˼������ʣ��������ʵ������д�±���
���� | ͬλ�� | ͬ�������� | ͬ���칹�� | ͬϵ�� |
��� | __ | __ | __ | __ |
�� ![]() ��
��![]() ��
�� ![]() ��
��![]() �۽��ʯ��ʯī ��12C��13C��14C ��
�۽��ʯ��ʯī ��12C��13C��14C ��![]() ��
��![]()
II����ͼ��A��B��C �ֱ����������Ľṹģ�ͣ�

��ش��������⣺
(1)A �ĵ���ʽ______________��B �Ľṹ��ʽ________________��
(2)A����ͬϵ��ķ���ʽ����ͨʽ_____________(�� n ��ʾ)���� n��____________ʱ��������ʼ����ͬ���칹�壻�� n=6 ʱ��ͬ���칹����__________�֡�
(3)A��B��C �����л����У�����ԭ�Ӿ��������___________(������)���ṹ��ʽΪ 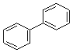 ���л����У�����ͬһƽ���ڵ�ԭ�������Ϊ__________������ ͬһƽ���ڵ�̼ԭ��������Ϊ____________��
���л����У�����ͬһƽ���ڵ�ԭ�������Ϊ__________������ ͬһƽ���ڵ�̼ԭ��������Ϊ____________��
(4)�л��� C �����еĽṹ��������_____________(����ĸ���)��
a����̼̼˫����̼̼��������Ľṹ b���ж���������ˮ���ܶȱ�ˮС
c������ʹ���� KMnO4 ��Һ����ˮ��Ӧ��ɫ d��һ������������������������Ӧ
(5)�������������л�����ȫȼ������ H2O �� CO2���������������(��ͬ״����)������_______(��A ��B �� C)��
III��ij�л���Ľṹ��ʽ��ͼ��1mol ���л��������Ժ�______mol������Ӧ�������Ժ�_____molNaOH ��Ӧ��
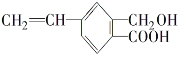
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ĸ���ͬ�������У��ڲ�ͬ�����½��кϳɰ���Ӧ��������������ͬʱ���ڲⶨ�Ľ���ж����ɰ�������������
A.v(H2)=0.1 mol��(L��min)-1B.v(N2)=0.1 mol��(L��min)-1
C.v(N2)=0.2 mol��(L��min)-1D.v(NH3)=0.3 mol��(L��min)-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. 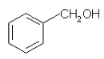 ��
��![]() ������ͬ�Ĺ����ţ���Ϊͬϵ��
������ͬ�Ĺ����ţ���Ϊͬϵ��
B. 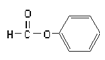 ����ȩ�࣬������Ϊ��CHO
����ȩ�࣬������Ϊ��CHO
C. ![]() ������Ϊ��2���һ���1����ϩ
������Ϊ��2���һ���1����ϩ
D. ![]() ������Ϊ��2������1��3������ϩ
������Ϊ��2������1��3������ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ���ѧϰ���ʽṹ�����ʵ���Ҫ���ߣ���ͼ��Ԫ�����ڱ���һ���֣������Ԫ�آ٩����ڱ��е�λ�ûش��������⡣
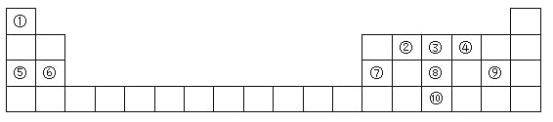
(1)�������ԭ�ӽṹʾ��ͼ��______________________��
(2)�ۡ��ܡ������̬�⻯���ȶ�����С�����˳���ǣ�(�ѧʽ)__________________��
(3)�ࡢ�������������Ӧˮ���������ǿ��˳���ǣ�(�ѧʽ)__________________��
(4)�ڡ�����Ԫ���γɵ�AB2�����ʵĵ���ʽ�ǣ�_______________________��
(5)�١��ܡ��ݡ����е�ijЩԪ�ؿ��γɼȺ����Ӽ��ֺ����ۼ��Ļ����д������һ�ֻ�����Ļ�ѧʽ��________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ���ѧϰ��ѧ����Ҫ����,������������Ϣ���ɡ��±����������ֶ�����Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼ�(��֪��Ԫ�ص�ԭ�Ӱ뾶Ϊ0.089 nm)��
Ԫ�ش��� | A | B | C | D | X | Y |
ԭ�Ӱ뾶/nm | 0.037 | 0.143 | 0.102 | 0.099 | 0.074 | 0.075 |
��Ҫ���ϼ� | +1 | +3 | +6,-2 | -1 | -2 | +5,-3 |
(1)CԪ�������ڱ��е�λ��Ϊ___�� �����ӽṹʾ��ͼΪ��____��
(2)B������������Ӧ��ˮ������Y������������Ӧ��ˮ���ﷴӦ�����ӷ���ʽΪ____��
(3)����C��D ����Ԫ��˵����ȷ����_________(�����)
a�������ӵİ뾶D>C b����̬�⻯����ȶ���D��Cǿ c������������Ӧ��ˮ���������C��Dǿ
(4)д����A��D��X����Ԫ����ɵ�ij�ֿ�������ɱ�����ʵĵ���ʽ_____________��
(5)�Ƚ�YԪ������ͬ�������Ԫ�ص��⻯����ȶ��� _______(���⻯�ﻯѧʽ)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com