
【题目】已知25℃时,CaSO4在水中的沉淀溶解平衡曲线,如图所示,向100mL该条件下的CaSO4饱和溶液中,加入400mL 0.01mol/L的Na2SO4溶液,针对此过程的下列叙述正确的是( ) 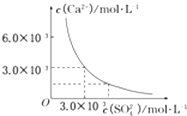
A.溶液中析出CaSO4沉淀,最终溶液中c(SO ![]() )较原来大
)较原来大
B.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO ![]() )都变小
)都变小
C.溶液中析出CaSO4沉淀,溶液中c(Ca2+)、c(SO ![]() )都变小
)都变小
D.溶液中无沉淀析出,但最终溶液中c(SO ![]() )较原来大
)较原来大
【答案】D
【解析】解:由图示可知,在该条件下,CaSO4饱和溶液中,c(Ca2+)=c( SO42﹣)=3.0×10﹣3 mol/L,Ksp(CaSO4)=9.0×10﹣6 . 当向100 mL该条件下的CaSO4饱和溶液中加入400 mL 0.01 mol/L的Na2SO4溶液后,混合液中c(Ca2+)= ![]() =6.0×10﹣4 mol/L,c(SO42﹣)=
=6.0×10﹣4 mol/L,c(SO42﹣)= ![]() =8.6×10﹣3 mol/L,溶液中c(Ca2+)c( SO42﹣ )=5.16×10﹣6<Ksp(CaSO4)=9.0×10﹣6 , 所以混合液中无沉淀析出,最终溶液中硫酸根离子浓度增大;故选D.
=8.6×10﹣3 mol/L,溶液中c(Ca2+)c( SO42﹣ )=5.16×10﹣6<Ksp(CaSO4)=9.0×10﹣6 , 所以混合液中无沉淀析出,最终溶液中硫酸根离子浓度增大;故选D.
通过图象分析得到该温度下硫酸钙饱和溶液中的沉淀溶解平衡为:CaSO4(s)Ca2++SO42﹣;c(Ca2+)=c( SO42﹣)=3.0×10﹣3 mol/L;
溶度积常数Ksp(CaSO4)=c(Ca2+)×c( SO42﹣)=9.0×10﹣6
通过计算混合溶液中钙离子浓度和硫酸根离子浓度,乘积与Ksp比较来判断沉淀的生成与溶解;


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】牛奶放置时间长了会变酸,这是因为牛奶中含有不少乳糖,在微生物的作用下乳糖分解而变成乳酸,乳酸的结构简式为 ![]() .已知有机物中若含有相同的官能团,则化学性质相似.完成下列问题:
.已知有机物中若含有相同的官能团,则化学性质相似.完成下列问题:
(1)写出乳酸分子中官能团的名称 .
(2)一定条件下乳酸能发生的反应类型有(填序号).
A.水解反应
B.取代反应
C.加成反应
D.中和反应
E.氧化反应
F.酯化反应
(3)写出乳酸与碳酸钠溶液反应的化学方程式 .
(4)乳酸在浓硫酸作用下,两分子相互反应生成链状结构的物质,写出此生成物的结构简式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1.000gFeC2O42H2O固体样品放在热重分析仪中进行热重分析,测得其热重分析曲线(样品质量随温度变化的曲线)如图所示:
已知:①草酸盐受热分解易放出碳的氧化物.②500℃之前,该热重分析仪的样品池处于Ar气气氛中,500℃时起,样品池与大气相通.完成下列填空:
(1)300℃时是样品脱水的过程,试确定350℃时样品是否脱水完全 △ (填“是”或“否”),判断的理由是什么?(要求写出推算过程).
(2)400℃时发生变化的化学方程式是 .
(3)将600℃时样品池中残留的固体隔绝空气冷却至室温,再向该固体中加入一定量的稀盐酸刚好完全溶解,用pH试纸测得所得溶液的pH=3,其原因是(用离子方程式回答).向该溶液中滴加适量NaOH溶液,生成红褐色沉淀,测得此时溶液中铁元素的离子浓度为4.0×10﹣11 molL﹣1 , 则此时溶液的pH=(已知:Ksp[Fe(OH)2]=8.0×10﹣16 , Ksp[Fe(OH)3]=4.0×10﹣38).
(4)将1500℃时样品池中残留的固体隔绝空气冷却后,用稀盐酸溶解得一棕黄色溶液.取少量该溶液滴加KSCN,溶液显血红色;另取少量该溶液滴加K3[Fe(CN)6](铁氰化钾)溶液,产生特征蓝色沉淀.试写出图中1 400℃时发生反应的化学方程式 , 产生特征蓝色沉淀的离子反应方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证铜与稀硝酸反应的还原产物是NO而不是NO2 . 某同学设计了如图所示的装置,下列叙述错误的是( ) 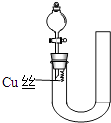
A.应先打开活塞和旋塞再从U型管右侧加入稀硝酸
B.加入的稀硝酸应充满U型管左侧
C.关闭旋塞后铜丝会全部溶解
D.反应停止后打开活塞,气体变成红棕色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED产品的使用为城市增添色彩.下图是氢氧燃料电池驱动LED发光的一种装置示意图.下列有关叙述正确的是( ) 
A.a处通入O2
B.b处为电池正极,发生了还原反应
C.通入O2的电极发生反应:O2+4e﹣+4H+=2H2O
D.该装置将化学能最终转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图用铜锌原电池(电解质溶液为稀硫酸)在铁棒上电镀铜,下列叙述正确的是( )

A. 铜在原电池中作负极,在电镀池中作阳极
B. 原电池溶液增加的质量比电镀池阴极增加的质量大
C. 锌棒每减少0.65 g,导线上转移的电子就为0.02 mol
D. 电镀池中的电解质溶液可用ZnSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=2的A、B两种酸溶液各1mL,分别加水稀释到1L(其pH与溶液体积V的关系如图所示),下列说法正确的是( ) ①a=5时,A是强酸,B是弱酸;
②若A、B都是弱酸,则5>a>2;
③稀释后,A酸溶液的酸性比B酸溶液强;
④A、B两种酸溶液的物质的量浓度一定相等.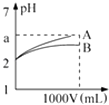
A.①②
B.③④
C.①③
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=2.6×10-9。该温度下,下列说法不正确的是( )
A. 同浓度的Na2SO4和Na2CO3混合溶液中滴加BaCl2溶液,BaSO4先析出
B. BaCO3的悬浊液中加入少量的新制氯水,c(Ba2+)增大
C. BaSO4和BaCO3共存的悬浊液中, 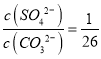
D. BaSO4悬浊液中加入Na2CO3浓溶液,BaSO4不可能转化为BaCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件.该小组同学为探究中毒原因进行了如下实验.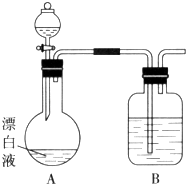
(1)小组同学依据漂白液具有漂白消毒的性质推测,漂白液中ClO﹣具有氧化性.实验如下:Ⅰ.用pH试纸检验,漂白液pH>7,饱和KAl(SO4)2溶液pH<7.
Ⅱ.取10mL漂白液,依次加入Na2SO3溶液和BaCl2溶液,有白色沉淀生成,经检验白色沉淀不溶于盐酸.
Ⅲ.另取10mL,漂白液,加入品红溶液,溶液红色逐渐变浅,一段时间后褪为无色.
Ⅳ.再取10mL漂白液,加入品红溶液,加入少量稀硫酸酸化后,溶液红色立即变为无色.
①漂白液pH大于7的原因是(用离子方程式表示) .
②由实验Ⅱ得出ClO﹣具有氧化性,写出反应的离子方程式 .
③对比实验Ⅲ和Ⅳ说明ClO﹣氧化性与溶液酸碱性的关系是 .
(2)小组同学依据(1)中的实验,提出:漂白液在酸性溶液中有Cl2生成.用如图所示的装置继续实验,探究漂白液在酸性溶液中是否能反应生成Cl2 . ①装置B的作用是 .
②若打开分液漏斗活塞向烧瓶中加入硫酸,不久烧瓶中有黄绿色气体产生.A中反应的离子方程式 .
③若打开分液漏斗活塞向烧瓶中加入饱和KAl(SO4)2溶液,首先观察到产生大量的白色胶状沉淀,不久烧瓶中有黄绿色气体产生.A中加KAl(SO4)2溶液反应的离子方程式是 .
(3)上述实验说明漂白液与酸性溶液混合会产生Cl2 . 若取10mL漂白液与足量BaCl2溶液混合后,不断通入SO2至过量,在实验过程中可能的实验现象是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com