
【题目】测定硫酸铜晶体(CuSO4xH2O)中x值的实验过程如下:

完成下列填空:
(1)必须要进行恒重操作的原因是___。
(2)下面是某同学的一次实验记录,请完成下表。
称量数据1 | 称量数据2 | 称量数据3 | 结晶水的X值 | 实验误差 |
11.685g | 13.691g | 12.960g | ____ | ____ |
(3)本次实验测得X值偏__(高、低),可能这次实验中产生误差的原因可能是___。
A.硫酸铜晶体中含有不挥发性杂质 B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去 D.加热失水后露置在空气中冷却
【答案】确保完全失去结晶水 5.096 1.92% 高 BC
【解析】
(1)确保完全失去结晶水,要求2次称量硫酸铜固体质量差小于0.001g;
(2)通过方程式CuSO4xH2O![]() CuSO4+xH2O计算;
CuSO4+xH2O计算;
(3)本次实验测得X值偏高;
(1)确保完全失去结晶水,要求2次称量硫酸铜固体质量差小于0.001g;
(2)m(CuSO4xH2O)=13.691g-11.685g=2.006g,m(H2O)=13.691g-12.960g=0.731g,
CuSO4xH2O![]() CuSO4+xH2O
CuSO4+xH2O
160+18x 18x
2.006 0.731
(160+18x):18x=2.006:0.731,化简求解,x=5.096;(5.096-5)/5×100%=1.92%;
(3)本次实验测得X值偏高;
A.硫酸铜晶体中含有不挥发性杂质,结晶水的质量偏小,则x偏低,与题意不符,A错误;
B.实验前晶体表面有湿存水,导致结晶水的质量偏大,则x偏高,符合题意,B正确;
C.加热时有晶体飞溅出去,导致结晶水的质量偏大,则x偏高,符合题意,C正确;
D.加热失水后露置在空气中冷却,结晶水的质量偏小,则x偏低,与题意不符,D错误;
答案为BC。


科目:高中化学 来源: 题型:
【题目】金属钛性能优越,被称为继铁、铝之后的“第三金属”。钛铁矿(主要成分为FeTiO3,含少量Fe2O3、SiO2等杂质)可用来制备TiO2,同时得到副产品绿矾(FeSO4·7H2O),工艺流程如图所示:
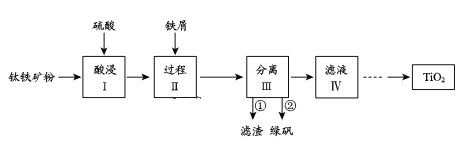
己知:①FeTiO3+2H2SO4=FeSO4+TiOSO4+2H2O
②TiO2+易水解,只能存在于强酸性溶液中
(1)酸浸I中Fe2O3与稀硫酸反应的离子方程式:_____。
(2)过程II中加入适量铁屑的目的是____。
(3)分离III中步骤②得到绿矾的操作是_____。
(4)由滤液IV提取TiO2的过程如下:
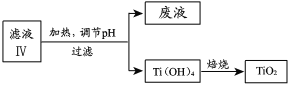
①请用化学平衡移动原理解释滤液加热煮沸的目的:______。
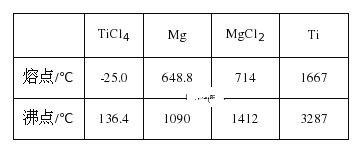
②由2Mg+TiCl4→Ti+2MgCl2反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据如表信息,需加热的温度略高于___℃即可。
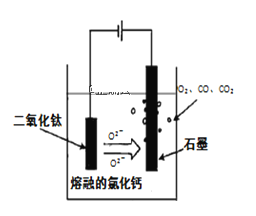
③电解TiO2制备钛的方法如图所示。该方法由于具备生产过程简化、生产成本低、产品质量高、环境友好等诸多优点而引人注目。已知TiO2熔融状态下不发生电离,电解时阴极反应式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写中正确的是
A.氢氧化镁与盐酸反应:H++OH-=H2O
B.铁与盐酸反应:2Fe+6H+=2Fe3++3H2
C.氧化铝溶于稀硫酸:Al2O3+6H+=2Fe3++3H2O
D.向沸水中滴加FeCl3溶液制备Fe(OH)3 胶体:Fe3++3H2O=Fe(OH)3+3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知硼与铝的性质相似,能与氧气、氢氧化钠溶液等物质反应,硼与氯气反应生成三氯化硼(BC13),生成的三氯化硼遇水水解产生白雾(已知:BC13的熔点为 -107. 3℃,沸点为12.5 ℃)。某兴趣小组设计如图所示装置制备三氯化硼。
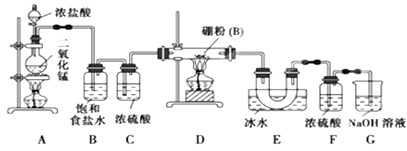
回答下列问题:
(1)写出装置A中发生反应的离子方程式________________。
(2)写出装置D中发生反应的化学方程式为_____________________。
(3)装置B、E的作用分别是________________、________________。
(4)可以用盛装____________(填试剂名称)的干燥管代替装置F和G,使实验更简便。
(5)为了顺利完成实验,点燃酒精灯的正确操作是______(填字母),
a.先点燃A处酒精灯,后点燃D处酒精灯
b.先点燃D处酒精灯,后点燃A处酒精灯
c.同时点燃A、D两处酒精灯
其理由是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】200mL Fe2(SO4)3溶液中含Fe3+56g,在该溶液中加入1mol/LBaCl2溶液300mL,反应后溶液中SO42-的物质的量浓度是(忽略混合后溶液的体积变化) ( )
A.7.5mol/LB.5mol/LC.6mol/LD.2.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.在硫酸工业的吸收塔中,采用浓硫酸吸收三氧化硫
B.Na2O2吸收CO2产生O2,可用作呼吸面具供氧剂
C.SO2与过量氨水反应得到![]()
D.无水CoCl2吸水会变为蓝色,可用于判断变色硅胶是否吸水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物X的结构简式如图所示,下列关于X的说法不正确的是
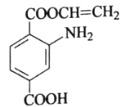
A.X分子中含有四种官能团
B.X能与金属钠反应,且相同条件下比水与金属钠反应要剧烈
C.1molX最多与5mol氢气发生加成反应
D.在一定条件下,X能发生加成、取代、加聚、缩聚、氧化、还原等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写出下列化学方程式:
(1)实验室可以用KClO3和浓盐酸反应制取氯气,写出发生反应的化学方程式并用双线桥表示电子转移方向和数目_____________。
(2)二氧化氯(ClO2)作为一种高效强氧化剂,可用KClO3和草酸(H2C2O4),稀硫酸,水浴加热制备。反应后产物中有ClO2、CO2和一种酸式盐,该反应的化学方程式为________________。
(3)写出工业上制备漂白粉的化学方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炼铅烟尘的主要成分为铅的氧化物(Pb2O3、Pb3O4、PbO)及PbSO4,其杂质主要为含镉(Cd)化合物,回收处理炼铅烟尘可实现资源再生。某工艺流程如图:
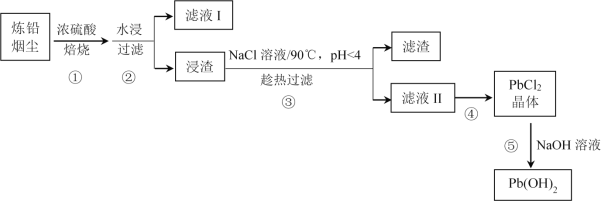
已知:ⅰ.Pb2O3![]() Pb3O4
Pb3O4![]() PbO
PbO
ⅱ.CdSO4易溶于水,热稳定性好
ⅲ.PbSO4(s)+2Cl-(aq)![]() PbCl2(s)+SO42-(aq)
PbCl2(s)+SO42-(aq)
PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq)
PbCl42-(aq)
ⅳ.Pb(OH)2为两性氢氧化物
(1)步骤①中焙烧的目的是________。在此过程中PbO与浓硫酸发生反应的化学方程式为________。
(2)滤液I的成分是________。
(3)相同反应时间,步骤①中焙烧温度和酸料比对Pb、Cd去除率的影响如下表所示(均未达到平衡状态)。
焙烧温度/℃ | 各元素的去除率/% | 酸料比/(mL/g) | 各元素的去除率/% | ||
Pb | Cd | Pb | Cd | ||
100 | 2.57 | 56.63 | 0.3 | 2.57 | 74.12 |
200 | 2.62 | 89.30 | 0.4 | 2.67 | 85.10 |
500 | 2.67 | 96.98 | 0.5 | 2.72 | 92.48 |
600 | 2.87 | 95.42 | 0.6 | 2.67 | 96.98 |
900 | 2.88 | 40.15 | 0.7 | 2.65 | 95.13 |
应选择的焙烧温度和酸料比为________。
Cd去除率随温度升高先增大后减小的原因可能为________。
(4)步骤③中NaCl溶液的作用是________。
(5)步骤④的操作是________。
(6)下列说法正确的是________(填序号)。
A.步骤①中浓硫酸作氧化剂
B.步骤③中pH<4的目的是防止Pb2+水解
C.步骤④的滤液可循环利用以提高Pb的回收率
D.步骤⑤中增大NaOH溶液浓度可使Pb沉淀完全
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com