
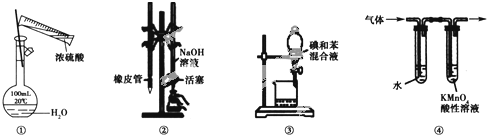
| A. | 图①所示装置进行浓硫酸稀释配制稀硫酸的实验 | |
| B. | 图②所示装置进行用已知浓度为NaOH溶液测定盐酸浓度的实验 | |
| C. | 图③所示装置进行用苯萃取碘水中碘的实验,并把碘的苯溶液从漏斗下口倒出 | |
| D. | 图④所示装置可检验溴乙烷发生消去反应得到的气体中含有乙烯 |
分析 A.不能在容量瓶中稀释浓硫酸;
B.氢氧化钠不能放在酸式滴定管中;
C.碘易溶于苯;
D.乙烯中混有乙醇,用水除杂,然后用酸性高锰酸钾检验.
解答 解:A.容量瓶只能用于配制溶液,且在常温下使用,不能在容量瓶中稀释浓硫酸,故A错误;
B.氢氧化钠可腐蚀玻璃,不能放在酸式滴定管中,故B错误;
C.碘易溶于苯,不能用分液的方法分离,故C错误;
D.溴乙烷在氢氧化钠的乙醇溶液中发生消去反应,乙烯中混有乙醇,乙醇易溶于水,用水除杂,然后用酸性高锰酸钾检验,故D正确.
故选D.
点评 本题考查较为综合,涉及气体的制备、溶液的配制,物质的分离以及检验等知识,为高考常见题型,侧重学生的分析能力和实验能力的考查,注意把握实验的可行性的评价,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ④⑤⑥ | C. | ②④⑥ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiH4的沸点高于CH4,可推测PH3的沸点也高于NH3 | |
| B. | CO2晶体是分子晶体,可推测SiO2晶体也是分子晶体 | |
| C. | PCl3 为三角锥形,可推测NF3也为三角锥形结构 | |
| D. | C2H6的碳链是直线型的,可推测C3H8的碳链也是直线型的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
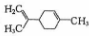 ,有关柠檬烯的分析正确的是( )
,有关柠檬烯的分析正确的是( )| A. | 一氯代物共有7种 | |
| B. | 分子中所有碳原子一定在同一平面 | |
| C. | 和丁基苯(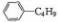 )互为同分异构体 )互为同分异构体 | |
| D. | 一定条件下,分别可以发生加成、取代、氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 至少含有4种离子 | |
| B. | 取少量原溶液先加入盐酸,后加入BaCl2溶液,肯定会产生白色沉淀 | |
| C. | 若原溶液中加入硝酸酸化的硝酸银溶液产生白色沉淀,则可推断溶液中含有K+ | |
| D. | 溶液中可能含有Fe3+、NH4+、SO42-、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用葡萄糖制镜或保温瓶胆 | B. | 用Na2S除去废水中的Hg2+ | ||
| C. | 用NaHCO3治疗胃酸过多 | D. | 用Na2SiO3溶液制备木材防火剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
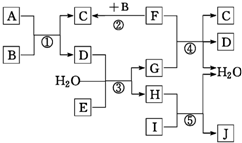 下列转化关系图中,A、B、C、D、E在常温下为气体,B、E、F为单质,其中F为黑色固体;C、D均能使澄清的石灰水变浑浊,D、E均能使品红溶液褪色;I是一种红棕色固体氧化物;反应④中固态F与G的浓溶液在加热时方能发生反应.回答下列问题:
下列转化关系图中,A、B、C、D、E在常温下为气体,B、E、F为单质,其中F为黑色固体;C、D均能使澄清的石灰水变浑浊,D、E均能使品红溶液褪色;I是一种红棕色固体氧化物;反应④中固态F与G的浓溶液在加热时方能发生反应.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com