
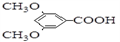
化合物M( )具有预防心血管疾病的作用,其一种合成路线如下:
)具有预防心血管疾病的作用,其一种合成路线如下:
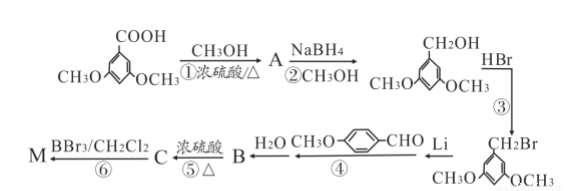
已知:RCH2Br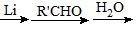


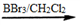
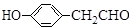
回答下列问题:
(1)M的官能团名称为_____________。③的反应类型是___________。
 核磁共振氢谱中不同化学环境的氢原子个数比为___________。
核磁共振氢谱中不同化学环境的氢原子个数比为___________。
(2)写出①的化学方程式____________________。
(3)B的结构简式为__________________。
(4) 有多种同分异构体,其中能发生银镜反应且苯环上一氯取代物只有两种的同分异构体有_________________种。
有多种同分异构体,其中能发生银镜反应且苯环上一氯取代物只有两种的同分异构体有_________________种。
(5)参照上述合成路线,设计由乙烯合成2-丁醇的合成路线(用合成路线流程图表示,并注明反应条件,合成过程中只有无机试剂可任选)_______________________。
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源:2016-2017学年江苏省扬州市宝应县高二下学期学业水平测试(三)化学试卷(解析版) 题型:选择题
下列实验装置、试剂选用或操作正确的是
A. 除去CO2中的HCl 
B. 干燥Cl2 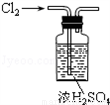
C. 稀释浓硫酸 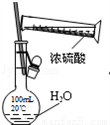
D. 制备少量O2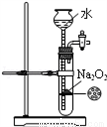
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省洛阳市高二(平行班)3月月考化学试卷(解析版) 题型:选择题
下列有机物的命名中,正确的是( )
A. 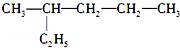 (2-乙基戊烷) B.
(2-乙基戊烷) B. 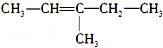 (3-甲基-2-戊烯)
(3-甲基-2-戊烯)
C.  (2-甲基-戊炔) D.
(2-甲基-戊炔) D.  (1-甲基-5-乙基苯)
(1-甲基-5-乙基苯)
查看答案和解析>>
科目:高中化学 来源:2017届陕西省西安市高三模拟(一)理综化学试卷(解析版) 题型:实验题
某红色固体粉末样品可能含有Fe2O3和Cu2O中的一种或两种,某化学兴趣小组对其组成进行探究。完成下列空格。
①提出假设:
假设1:只存在Fe2O3;假设2:_________;假设3:既存在Fe2O3也存在Cu2O。
②查找资料:Cu2O在酸性溶液中会发生反应:Cu2O+2H+=Cu+Cu2++H2O。
③实验方案设计与分析:
方案一:步骤一:取少量样品于烧杯中,加入过量浓硝酸,产生一种红棕色的气体。由此可得出假设____不成立,写出产生上述气体的化学方程式___________________。
步骤二:取少量步骤一溶液置于试管中滴加_______,振荡,若________,则说明假设3成立。
方案二:
取少量样品于烧杯中,加入过量稀硫酸,若固体全部溶解,说明假设_不成立。
方案三:
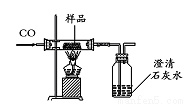
同学们设计了如下实验方案测定该样品中Fe2O3的质量分数(装置气密性良好,假设样品完全反应):
步骤一:取样品并称量该样品的质量为m1;
步骤二:测出反应前广口瓶和瓶内物质总质量m2;
步骤三:测出反应后广口瓶和瓶内物质总质量m3;
步骤四:计算得出矿物样品中Fe2O3的质量分数。
讨论分析:该实验方案________(填“能”或“不能”)测出矿物中Fe2O3的质量分数。不改变装置和药品,通过计算得出矿物中Fe2O3的质量分数,你还可以通过测定_______。若测得m1为3.04g,m3=m2+1.76g,则原样品中Fe2O3的质量分数为_____(结果保留四位有效数字)。
查看答案和解析>>
科目:高中化学 来源:2017届陕西省西安市高三模拟(一)理综化学试卷(解析版) 题型:选择题
下列关于有机化合物的叙述正确的是
A. 氟利昂-12的结构式为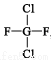 ,该分子是平面型分子
,该分子是平面型分子
B. 苯与液溴混合后撤入铁粉发生了加成反应
C. 分子式为C4H9Cl的同分异构体共有4种
D. 1mol苹果酸(HOOCCHOHCH2COOH)可与3molNaHCO3发生反应
查看答案和解析>>
科目:高中化学 来源:2017届天津市高三第四次月考化学试卷(解析版) 题型:选择题
下列操作和结论正确的是( )
A. 向淀粉水解后的溶液中滴加碘水,即可检验淀粉是否水解
B. NaAlO2溶液中滴加Na2CO3溶液,有沉淀和气体生成
C. 将SO2分别通入硝酸钡溶液和溶有氨气的氯化钡溶液中产生的沉淀成分不同
D. 用铂丝蘸取少量试液进行焰色反应,火焰呈黄色的一定是钠盐溶液
查看答案和解析>>
科目:高中化学 来源:2017届江苏省苏州市高三上学期期末考试化学试卷(解析版) 题型:推断题
以下流程是合成环烷烃的方法之一。
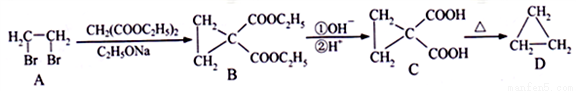
(1)B、C中含氧官能团的名称分别为____________、_______________。
(2)A→B的反应类型是____________。
(3)写出C→D反应的化学方程式__________________________________。
(4)写出同时满足下列条件的B的一种同分异构体的结构简式:____________
①分子中含三元环; ②分子中无甲基;③有4种不同化学环境的氢;④可发生银镜反应。
(5)请以1,3-丁二烯和CH2(COOC2H5)2、C2H5ONa为原料制备 ,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省扬州市高二下学期学业水平测试(二)化学试卷(解析版) 题型:简答题
碱式碳酸铜可用于生产木材防腐剂等。工业上可用微蚀刻废液(含有一定量Cu2+、H+、SO42-、H2O2和微量Fe3+)制备高纯度碱式碳酸铜,其制备过程如下:
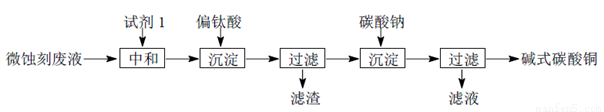
(1)试剂1最好选用________________。
a.Fe2O3 b.CaCO3 C.CuO
(2)加入Na2CO3沉淀前须除去Fe3+,否则Fe2(SO4)3会与Na2CO3反应,产生一种气体,同时生成NaFe3(OH)6(SO4)2沉淀,影响产品质量,写出该反应的化学方程式______________________。
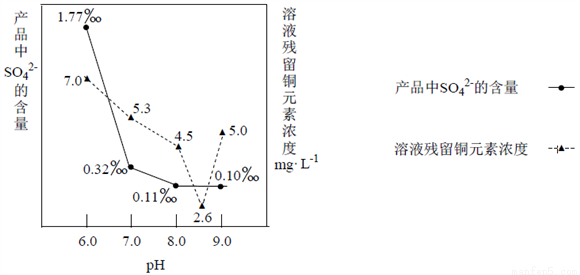
(3)加入Na2CO3沉淀时,反应液pH对产品中SO42-的含量以及反应液中Cu2+沉淀效率的影响如下图所示,第二次沉淀时溶液pH最好控制在___________________________。
(4)所制得的碱式碳酸铜的组成可表示为:xCuCO3·yCu(OH)2·zH2O,要测定其组成,甲同学设计的实验方案中需要如下五个步骤:①称取12.0克的样品;②高温分解;③测出生成CO2的质量为2.2克;④测出生成水蒸气的质量为1.8克;⑤称量生成CuO的质量为8.0克。而乙同学认为除步骤②外,实验只需测定四个量中的部分数据即可,则合理的组合为______________(填序号,写一组即可)。根据你的选择,计算出碱式碳酸铜的组成,写出计算过程。____________________________。
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三3月高考模拟化学试卷(解析版) 题型:选择题
配制物质的量浓度为0.1mol•L-1的Na2CO3溶液100 mL时,下列操作正确的是
A. 用托盘天平称取1.06 g 无水碳酸钠,在烧杯中加适量水溶解,待冷却到室温后,将溶液转移到容量瓶中
B. 在使用容量瓶前必须检查容量瓶是否完好以及瓶塞处是否漏水
C. 定容时,若加水超过刻度线,可用胶头滴管小心吸出多余部分
D. 定容时,若仰视,则所配溶液的浓度将偏高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com