
【题目】下列有关配合物的论述不合理的是
A.Na[Al(OH)4]和[Ag(NH3)2]OH都是配合物
B.Na3[AlF6]、Na2[SiF6]和[Cu(NH3)4]Cl2的配位数都是6
C.[ZnCl4]2-的空间构型为正四面体形
D.配合物[Cr(H2O)4Br2]Br·2H2O中,中心离子的化合价为+3价,配离子带1个单位的正电荷
科目:高中化学 来源: 题型:
【题目】(1)氨气是化学实验室常需制取的气体。实验室制取氨气通常有两种方法:
方法一 固体氢氧化钙与氯化铵共热
方法二 固体氢氧化钠与浓氨水反应
①下面的制取装置图中,方法一应选用装置________(填“A”或“B”,下同),方法二应选用装置________。
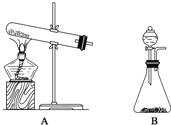
②写出加热NH4Cl和Ca(OH)2制取NH3的反应方程式_________。
③在制取后,如果要干燥氨气,应选用的干燥剂是_____,收集氨气的方法是______。
A.浓硫酸 B.碱石灰 C.五氧化二磷
D.向上排空气法 E.排水法 F.向下排空气法
④检验是否收集满氨气的方法是____________________________________。
(2)请观察如图装置,回答下列问题:
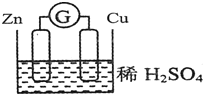
①负极是_______,发生_______反应(填氧化或还原)。
②正极的电极反应式_______。
③该装置是一种把_______________________的装置,当导线中有0.2 mol e-发生转移时,求参加氧化反应的物质的物质的量为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤烟气的脱硫脱硝是目前研究的热点。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) △H= -574 kJmol-1
②CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) △H= -1160 kJmol-1
③H2O(g) = H2O(l) △H= -44 kJmol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O( l ) 的热化学方程式_____________。
(2)某科研小组研究臭氧氧化--碱吸收法同时脱除SO2和NO工艺,氧化过程反应原理及反应热、活化能数据如下:
反应Ⅰ:NO(g)+ O3(g) ![]() NO2(g)+O2(g) △H1 = -200.9 kJmol-1 Ea1 = 3.2 kJmol-1
NO2(g)+O2(g) △H1 = -200.9 kJmol-1 Ea1 = 3.2 kJmol-1
反应Ⅱ:SO2(g)+ O3(g)![]() SO3(g)+O2(g) △H2 = -241.6 kJmol-1 Ea2 = 58 kJmol-1
SO3(g)+O2(g) △H2 = -241.6 kJmol-1 Ea2 = 58 kJmol-1
已知该体系中臭氧发生分解反应:2O3(g) ![]() 3O2(g)。请回答:
3O2(g)。请回答:
其它条件不变,每次向容积为2L的反应器中充入含1.0 mol NO、1.0 mol SO2的模拟烟气和2.0 mol O3,改变温度,反应相同时间t后体系中NO和SO2的转化率如图所示:

①由图可知相同温度下NO的转化率远高于SO2,结合题中数据分析其可能原因_______。
②下列说法正确的是________。
A.P点一定为平衡状态点
B.温度高于200℃后,NO和SO2的转化率随温度升高显著下降、最后几乎为零
C.其它条件不变,若缩小反应器的容积可提高NO和SO2的转化率
③假设100℃时P、Q均为平衡点,此时反应时间为10分钟,发生分解反应的臭氧占充入臭氧总量的10%,则体系中剩余O3的物质的量是________mol;NO的平均反应速率为________;反应Ⅱ在此时的平衡常数为_______________。
(3)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能:

①M极发生的电极反应式为___________________。
②当外电路通过0.2 mol电子时,质子交换膜左侧的溶液质量_____(填“增大”或“减小”)____克。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某红色固体粉末样品可能含有Fe2O3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究。
查阅资料:Cu2O在酸性溶液中会发生反应:Cu2O+2H+=Cu+Cu2++H2O
探究一:用如图所示装置进行实验,回答下列问题:
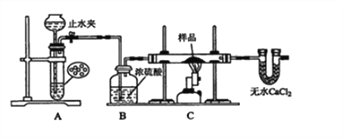
(1)仪器组装完成后,夹好止水夹,______________________ ,则说明装置A的气密性良好。
(2)装置A是氢气的发生装置,可以选用的药品是______(填选项)
A.稀硫酸和锌片 B.稀硝酸和铁片
C.氢氧化钠溶液和铝片 D.浓硫酸和镁片
(3)从下列实验步骤中,选择正确的操作顺序:①____________③(填序号)。
①打开止水夹
②熄灭C处的酒精喷灯
③C处冷却至室温后,关闭止水夹
④点燃C处的酒精喷灯
⑤收集氢气并验纯
⑥通入气体一段时间,排尽装置内的空气
探究二:
(4)甲同学取少量样品于试管中,加入适量的稀硫酸,若无红色物质生成,则说明样品中不含Cu2O;乙同学认为观点不正确,其原因是_____________(用离子方程式表示);丙同学另取少量样品于试管中,加入适量的浓硝酸,产生红棕色的气体.证明样品中一定含有________,其反应的离子方程式为_____;丁同学设计实验证明另一种物质是否存在,则其设计方案中检验另一种物质所有试剂名称为______________。
(5)取一定量样品于烧杯中,加入足量的稀硫酸,若反应后经过滤得到固体3.2g,滤液中Fe2+有1.0mol,则样品中n(Cu2O)=_________mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图装置中发生反应的离子方程式为:Zn+2H+=Zn2++H2↑。下列说法错误的是( )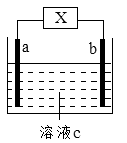
A.a、b不可能是同种材料的电极
B.X为电流计,c为稀盐酸,该装置为原电池
C.X为直流电源,c为稀硫酸,该装置为电解池
D.X为电流计,c为稀硫酸,a可能为铜电极,b可能为锌电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组用如图装置进行实验,试回答下列问题: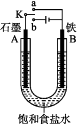
(1)若开始时开关K与a连接,则B极的电极反应为。
(2)若开始时开关K与b连接,则B极的电极反应为 , 总反应的离子方程式为。
(3)有关上述实验,下列说法正确的是。
A.溶液中Na+向A极移动
B.从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
C.反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
D.若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(4)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。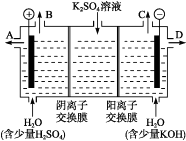
①该电解槽的阳极反应为。 此时通过阴离子交换膜的离子数(填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从出口(填“A”、“B”、“C”或 “D”)导出。
③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)已知有机物:
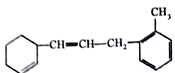
(1)该物质苯环上的一氯代物有_____种。
(2)1mol该物质和溴水混合,消耗Br2的物质的量为_____mol。
(3)1mol该物质和H2发生加成反应最多消耗H2______mol。
(4)下列说法不正确的是________(填序号)。
A.此物质可发生加聚、加成、取代、氧化等反应
B.1mol该物质中有2mol苯环
C.使溴水褪色的原理与乙烯相同
D.能使酸性KMnO4溶液褪色,发生的是加成反应
(Ⅱ)某有机物A化学式为CxHyOz,15gA完全燃烧可生成22gCO2和9gH2O。试求:
(5)该有机物的最简式________________。
(6)若A的相对分子质量为60且和Na2CO3混合有气体放出,A和醇能发生酯化反应,则A的结构简式为___________。
(7)若A的相对分子质量为60且是易挥发有水果香味的液体,能发生水解反应,则其结构简式为____________。
(8)若A分子结构中含有6个碳原子,具有多元醇和醛的性质,是人体生命活动的一种重要物质。则其结构简式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B两种有机物,当混合物的质量一定时,无论A、B以任意比例混合,完全燃烧时产生的CO2的量均相等,则符合上述条件的是
①同分异构体②同系物③具有相同的最简式④含碳的质量分数相同。
A. ①③ B. ②④ C. ①③④ D. ①②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com