
| A. | 无法判断该溶液中是否含有K+ | |
| B. | 该溶液中一定含有K+、SiO32-,可能含有CO32- | |
| C. | 该溶液中无SO32-,一定含有CO32- | |
| D. | 该溶液中可能含有K+和CO32- |
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:解答题
 J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期及中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等:M 是地壳中含虽最多的金属元素.请用化学用语填空..
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期及中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等:M 是地壳中含虽最多的金属元素.请用化学用语填空..| J | ||||
| R |
 .
.| 选项 | A | B | C | D |
| M | 温度 | 温度 | H2的物质的量 | 甲的物质的量 |
| N | 甲的物质的量 | 平衡常数K | 甲的转化率 | 生成物总物质的量 |
| 甲转化为HLO3的情况 | X取值范围 | N(HLO3)y/mol |
| 无HLO3的生成 | y=0 | |
| 有部分HLO3的生成 | ||
| 全部生成HLO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 |
| 操作步骤 | 现象 |
| 步骤1:向2mL 0.005mol•L-1 AgNO3溶液中加入2mL 0.005mol•L-1KSCN溶液,静置. | 出现白色沉淀. |
| 步骤2:取1mL上层清液于试管中,滴加1滴2mol•L-1 Fe(NO3)3溶液. | 溶液变红色. |
| 步骤3:向步骤2的溶液中,继续加入5滴3mol•L-1AgNO3溶液. | 出现白色沉淀,溶液红色变浅. |
| 步骤4:向步骤1余下的浊液中加入5滴3mol•L-1KI溶液. | 出现黄色沉淀. |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
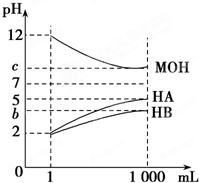 某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验:将pH=2的两种酸溶液HA、HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题:
某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验:将pH=2的两种酸溶液HA、HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和乙醚互为同分异构体 | |
| B. | 乙醇和乙二醇互为同系物 | |
| C. | 含羟基的化合物一定属于醇类 | |
| D. | 等质量的乙醇、乙二醇与足量钠反应时,乙二醇产生的氢气的量较乙醇的多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
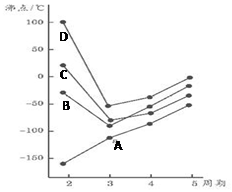 如图为四、五、六、七主族元素简单氢化物沸点随周期变化图象,(A、B、C、D代表氢化物中另外一种元素)分析图象,下列说法正确的是( )
如图为四、五、六、七主族元素简单氢化物沸点随周期变化图象,(A、B、C、D代表氢化物中另外一种元素)分析图象,下列说法正确的是( )| A. | A元素氧化物晶体中存在分子间作用力 | |
| B. | A、B、C、D非金属性由小到大的顺序是:A<B<D<C | |
| C. | D的氢化物固态比液态时密度大 | |
| D. | B元素一种氢化物可做火箭的染料,为CH4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com