
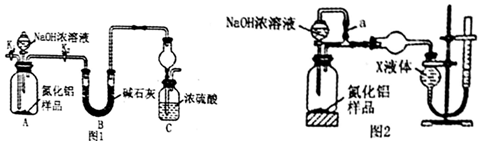
·ÖĪö £Ø1£©°±ĘųŹĒŗĶÅØĮņĖįÄÜ·¢Éś·“Ó¦µÄĘųĢ壬Ņ×·¢Éśµ¹Īü£»
£Ø2£©×é×°ŗĆŹµŃé×°ÖĆ£¬ŅĄ¾ŻŌĄķæÉÖŖĘųĢåÖʱøŠčŅŖĻČ¼ģ²é×°ÖĆĘųĆÜŠŌ£¬¼ÓČėŹµŃéŅ©Ę·£®½ÓĻĀĄ“µÄŹµŃé²Ł×÷ŹĒ¹Ų±ÕK1£¬“ņæŖK2£¬·“Ӧɜ³É°±ĘųŗóĪĄ°Ń×°ÖĆÖŠµÄĘųĢåČ«²æøĻČė×°ÖĆC±»ÅØĮņĖįĪüŹÕ£¬×¼Č·²ā¶Ø×°ÖĆCµÄŌöÖŲ¼ĘĖć£»
£Ø3£©×°ÖĆ“ęŌŚČ±ĻŻŹĒæÕĘųÖŠµÄĖ®ÕōĘųŗĶ¶žŃõ»ÆĢ¼Ņ²æÉŅŌ½ųČė×°ÖĆC£¬Ź¹²ā¶Ø½į¹ūĘ«øߣ¬ŠčŅŖĮ¬½ÓŅ»øöŹ¢¼īŹÆ»ŅøÉŌļ¹Ü£»
£Ø4£©°±Ęų¼«Ņ×ČÜÓŚĖ®£¬ĮæĘų×°ÖĆÖŠµÄXŅŗĢå²»ÄÜÓė°±Ęų·“Ó¦£¬²»ÄÜŹ¹°±ĘųČܽā£»
£Ø5£©ŅĄ¾ŻAIN+NaOH+H2OØTNaAIO2+NH3”üŌŚ¶ØĮæ¹ŲĻµ¼ĘĖć£»Čē¹ū½«a“¦¼Š×”£¬ŌņµĪ¼ÓµÄŅŗĢåĢå»żŅ²»įÅųöŅ»¶ØĮæµÄŅŗĢ壬ĖłŅŌµ¼ÖĀ²āµĆµÄĘųĢåĢå»żĘ«“ó£®
½ā“š ½ā£ŗ£Ø1£©°±ĘųŹĒÓėÅØĮņĖįÄÜ·¢Éś·“Ó¦µÄĘųĢ壬Ņ×·¢Éśµ¹Īü£¬Ķ¼C×°ÖĆÖŠĒņŠĪøÉŌļ¹ÜµÄ×÷ÓĆŹĒ·ĄÖ¹µ¹ĪüµÄ×÷ÓĆ£¬
¹Ź“š°øĪŖ£ŗ·ĄÖ¹µ¹Īü£»
£Ø2£©×é×°ŗĆŹµŃé×°ÖĆ£¬ŠčŅŖĻČ¼ģ²é×°ÖĆĘųĆÜŠŌ£¬¼ÓČėŹµŃéŅ©Ę·£®½ÓĻĀĄ“µÄŹµŃé²Ł×÷ŹĒ¹Ų±ÕK1£¬“ņæŖK2£¬“ņæŖ·ÖŅŗĀ©¶·»īČū£¬¼ÓČėNaOHÅØČÜŅŗ£¬ÖĮ²»ŌŁ²śÉśĘųĢ壮“ņæŖK1£¬ĶØČėµŖĘųŅ»¶ĪŹ±¼ä£¬²ā¶ØC×°ÖĆ·“Ó¦Ē°ŗóµÄÖŹĮæ±ä»Æ£®ĶØČėµŖĘųµÄÄæµÄŹĒ£¬·“Ӧɜ³É°±ĘųŗóĪĄ°Ń×°ÖĆÖŠµÄĘųĢåČ«²æøĻČė×°ÖĆC±»ÅØĮņĖįĪüŹÕ£¬×¼Č·²ā¶Ø×°ÖĆCµÄŌöÖŲ¼ĘĖć£¬
¹Ź“š°øĪŖ£ŗ¼ģ²é×°ÖĆĘųĆÜŠŌ£»¹Ų±ÕK1£¬“ņæŖK2£»°Ń×°ÖĆÖŠ²ŠĮōµÄ°±ĘųČ«²æøĻČėC×°ÖĆ£»
£Ø3£©×°ÖĆ“ęŌŚČ±ĻŻŹĒæÕĘųÖŠµÄĖ®ÕōĘųŗĶ¶žŃõ»ÆĢ¼Ņ²æÉŅŌ½ųČė×°ÖĆC£¬Ź¹²ā¶Ø½į¹ūĘ«øߣ¬ŠčŅŖĮ¬½ÓŅ»øöŹ¢¼īŹÆ»ŅøÉŌļ¹Ü£¬
¹Ź“š°øĪŖ£ŗC×°ÖĆ³öæŚ“¦Į¬½ÓŅ»øöøÉŌļ×°ÖĆ£»
£Ø4£©a£®CCl4²»ÄÜČܽā°±Ęų£¬æÉŅŌÓĆÅÅĖÄĀČ»ÆĢ¼ČÜŅŗµÄ·½·Ø²ā¶Ø°±ĘųĢå»ż£¬¹ŹaÕżČ·£»
b£®°±Ęų¼«Ņ×ČÜÓŚĖ®£¬²»ÄÜÅÅĖ®·Ø²ā¶Ø£¬¹Źb“ķĪó£»
c£®°±Ęų¼«Ņ×ČÜÓŚĖ®£¬²»ÄÜÓĆÅÅNH4ClČÜŅŗµÄ·½·Ø²ā¶ØĘųĢåĢå»ż£¬¹Źc“ķĪó£»
d£®°±Ęų²»ČÜÓŚ±½£¬æÉŅŌĄūÓĆÅű½ČÜŅŗ£¬²ā¶Ø°±ĘųµÄĢå»ż£¬¹ŹdÕżČ·£»
¹Ź“š°øĪŖ£ŗad£»
£Ø5£©Čōm gѳʷĶźČ«·“Ó¦£¬²āµĆÉś³ÉĘųĢåµÄĢå»żĪŖV mL£ØŅŃ×Ŗ»»ĪŖ±ź×¼×“æö£©£¬
AlN+NaOH+H2OØTNaAIO2+NH3”ü
41 22.4L
m V”Į10-3L
m=$\frac{41V”Į1{0}^{-3}}{22.4}$g£¬ŌņAlNµÄÖŹĮæ·ÖŹż=$\frac{41V”Į1{0}^{-3}}{22.4m}$”Į100%=$\frac{41V}{22400m}$”Į100%£¬Čē¹ū½«a“¦¼Š×”£¬×°ÖĆÄŚŃ¹Ēæ±ä»ÆŌņµĪ¼ÓµÄŅŗĢåĢå»żŅ²»įÅųöŅ»¶ØĮæµÄŅŗĢ壬ĖłŅŌµ¼ÖĀ²āµĆµÄĘųĢåĢå»żĘ«“ó£¬
¹Ź“š°øĪŖ£ŗ$\frac{41V}{22400m}$”Į100%£»Ę«“ó£®
µćĘĄ ±¾Ģāæ¼²éĮĖĪļÖŹŗ¬ĮæµÄ²ā¶ØĢ½¾æŹµŃéÉč¼ĘŗĶŹµŃé·ÖĪöÅŠ¶Ļ£¬°ŃĪÕŹµŃ黳±¾²Ł×÷ŗĶĪļÖŹŠŌÖŹŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£¬×¢Ņā°ŃĪÕŹµŃéŌĄķŅŌ¼°ø÷²æ²Ł×÷µÄÄæµÄ£¬²ąÖŲÓŚæ¼²éѧɜµÄŹµŃéÄÜĮ¦ŗĶ¼ĘĖćÄÜĮ¦£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ĘÕĀŽÅĮĶŖ·Ö×ÓÖŠÓŠ2øöŹÖŠŌĢ¼Ō×Ó | |
| B£® | æÉÓĆäåĖ®»ņFeCl3ČÜŅŗ¼ų±šXŗĶY | |
| C£® | ŌŚÓŠ»śĪļXµÄ1HŗĖ“Ź²ÕńĘ×Ķ¼ÖŠ£¬ÓŠ4×éĢŲÕ÷·å£¬1mol X ×ī¶ąæÉŅŌĻūŗÄ1mol NaOH | |
| D£® | X”¢YŗĶĘÕĀŽÅĮĶŖ¶¼ÄÜ·¢Éś¼Ó³É”¢Ė®½ā”¢Ńõ»Æ”¢ĻūČ„·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆĒā·śĖį¶Ō²£Į§½ųŠŠæĢŹ“æÉÖĘ³ÉÉĶŠÄŌĆÄæµÄµń»Ø²£Į§ | |
| B£® | Na2CO3·ŪÄ©ÓöĖ®Éś³Éŗ¬ÓŠ½į¾§Ė®µÄĢ¼ĖįÄĘ¾§Ģ壬øĆ¾§ĢåŅ»¶ØŹĒNa2CO3•10H2O | |
| C£® | ĀČĖ®ŗĶøÉŌļµÄĀČĘų¾łÄÜŹ¹ĻŹ»ØĶŹÉ« | |
| D£® | ŗĻ½šµÄÓ²¶ČæÉŅŌ“óÓŚĖüµÄ“潚Źō²æ·Ö£¬ŗĻ½šµÄČŪµćŅ²æÉŅŌµĶÓŚĖüµÄ³É·Ö½šŹō |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀĻĀ£¬½«pH=2µÄŃĪĖįŗĶpH=12µÄ°±Ė®µČĢå»ż»ģŗĻ£ŗc£ØNH4+£©£¾c£ØCl-£©£¾c£ØOH-£©£¾c£ØH+£© | |
| B£® | 0.1mol•L-1 Na2CO3ČÜŅŗ£ŗ2c£ØNa+£©=c£ØHCO3-£©+c£ØCO32-£©+c£ØH2CO3£© | |
| C£® | ĻąĶ¬ĪĀ¶ČĻĀ£¬0.6 mol/L°±Ė®ČÜŅŗÓė0.3 mol/L°±Ė®ČÜŅŗÖŠc£ØOH-£©Ö®±ČŹĒ2£ŗ1 | |
| D£® | ĪļÖŹµÄĮæÅضČĻąµČµÄ¢ŁNH4HSO4ČÜŅŗ”¢¢ŚNH4HCO3ČÜŅŗ”¢¢ŪNH4ClČÜŅŗÖŠ£¬c£ØNH4+£©µÄ“󊔹ŲĻµ£ŗ¢Ł£¾¢Ś£¾¢Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1L 1mol•L-1µÄŃĪĖįČÜŅŗÖŠ£¬Ėłŗ¬ĀČ»ÆĒā·Ö×ÓŹżĪŖNA | |
| B£® | 11.2LŃõĘųÖŠĖłŗ¬ÓŠµÄŌ×ÓŹżĪŖNA | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ42gŅŅĻ©ŗĶ¶”Ļ©»ģŗĻĘųĢåÖŠ£¬¼«ŠŌ¼üŹżĪŖ6NA | |
| D£® | 1L0£®lmol/L µÄ Fe2£ØSO4£©3 ČÜŅŗÖŠ£¬Fe3+µÄŹżÄæĪŖ 0.2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆĖÄĀČ»ÆĢ¼ŻĶČ”µāĖ®£¬ĻĀ²ćČÜŅŗ³Ź×ĻÉ« | |
| B£® | ¼ÓČėĀČ»Æ±µČÜŅŗÓŠ°×É«³Įµķ²śÉś£¬ŌŁ¼ÓŃĪĖį£¬³Įµķ²»ĻūŹ§£¬Ņ»¶ØÓŠSO42- | |
| C£® | ĶłĀČ»ÆĢśČÜŅŗÖŠ¼ÓČėĒāŃõ»ÆÄĘČÜŅŗæÉÖʵĆĒāŃõ»ÆĢś½ŗĢå | |
| D£® | ijČÜŅŗµĪ¼Ó×ĻÉ«ŹÆČļŹŌ¼Į³ŹŗģÉ«£¬øĆČÜŅŗŅ»¶Øŗ¬ÓŠÄ³ÖÖĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ĻÖÓŠ14.4gCOŗĶCO2µÄ»ģŗĻĘųĢ壬ŌŚ±ź×¼×“æöĻĀĖłÕ¼µÄĢå»żŌ¼ĪŖ8.96L£®»Ų“šĻĀĮŠĪŹĢā£ŗ
ĻÖÓŠ14.4gCOŗĶCO2µÄ»ģŗĻĘųĢ壬ŌŚ±ź×¼×“æöĻĀĖłÕ¼µÄĢå»żŌ¼ĪŖ8.96L£®»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com