
【题目】下列物质的水溶液中,加入Ba(OH)2溶液后,原溶液中阴、阳离子都减少的是( )
A.CuSO4
B.Ca(NO3)2
C.Na2CO3
D.FeCl3
科目:高中化学 来源: 题型:
【题目】水中的溶解氧的含量是衡量水质的一个重要指标,某实验兴趣小组通过如下步骤来测量水中溶解氧的含量:
步骤一:向溶解氧测量瓶中注入20.00 mL水样,再分别加入1 mL 0.1 mol L-1MnSO4溶液和3mL NaOH和KI的混合溶液,充分反应。此时发生反应的化学方程式为: Mn2++2OH-=Mn(OH)2↓ 2Mn(OH)2+ O2 =2MnO(OH)2
步骤二:向上述混合物中加入1.5 mL浓硫酸,充分反应后制沉淀完全溶解,此时溶液呈黄色。
步骤三:将溶液全部转移到容量瓶中,向其中滴加23滴淀粉溶液,溶液呈蓝色。用 0.005 mol L-1的Na2S2O3标准溶液滴定至蓝色恰好消失,共消耗Na2S2O3标准溶液3.60 mL。此时发生反应为:
I2+2Na2S2O3= 2NaI + Na2S4O6
(1)25 ℃时,步骤一中当加入NaOH使溶液的pH = 12时,此时溶液中的c(Mn2+)=_________mol L-1 。 (已知 KspMn(OH)2 =2.06×10-13)
(2)写出步骤二中所发生反应的化学方程式:______________________________。
(3)计算该水样中溶解氧的含量。(单位:mg L-1,请写出计算过程)______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如下图所示装置进行试验
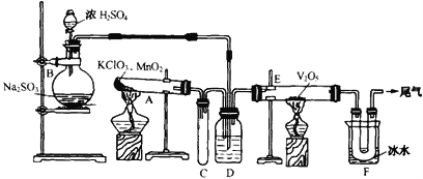
(1)烧瓶B内发生反应的化学方程式是________________。在本实验中,往往选择质量分数75%左右的浓硫酸,试分析其原因________________。
(2)小试管C的作用是________________。
(3)广口瓶D内盛的试剂是____________,装置D的3个作用是:①_________、②_______、③_________。
(4)玻璃管E内发生反应的化学方程式是________________。
(5)装置F中U形管中所收集物质的成分是________________。
(6)若U形管内收集到的物质很少,分析其原因不可能是______________(填序号)。
a、装置气密性不好
b、制得的SO2中混有少量H2S杂质使催化剂中毒;
c、气流速度过快。
(7)从U形管导出的尾气的处理方法是________________,相关反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将某一元弱酸(HA)和氢氧化钠溶液混合后溶液呈中性,则此溶液中c(Na+)与c(A-)的关系为( )
A. c(Na+)=c(A-) B. c(Na+)<c(A-) C. c(Na+)>c(A-) D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯催化氧化成乙醛可设计成如图所示的燃料电池,其总反应为:2CH2=CH2+O2→2CH3CHO。下列有关说法正确的是

A.该装置能量转化形式是电能转化为化学能
B.负极反应式为:CH2=CH2-2e-+H2O=CH3CHO +2H+
C.每有0.1 mol O2反应,则向负极迁移的H+的物质的量为0.4 mol
D.电子移动方向:电极a→磷酸溶液→电极b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某合作学习小组讨论辨析以下说法:①粗盐和矿泉水都是混合物;②氨水和NaOH都是电解质;③冰和干冰既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱;⑦豆浆和烟、雾都是胶体。上述说法正确的是( )
A.①②③④ B.①②④⑥ C.①③④⑦ D.③⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体区别于其它分散系的本质是( )
A.胶体粒子带电荷并且在一定条件下能稳定存在
B.胶体粒子不能穿过半透膜,能通过滤纸空隙
C.胶体的分散质粒子直径在1nm~100nm之间
D.胶体粒子能够发生布朗运动而且能产生丁达尔现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1911年,科学家发现汞在4.2K以下时电阻突然趋近于零——即低温超导性。1986年,科学家又发现了Nb3Ge在23K下具有超导性。1987年2月,赵忠贤及合作者独立发现了在液氮温区(沸点77K)的高温超导体,其晶胞如图所示,元素组成为Ba-Y-Cu-O(临界温度93K),推动了国际高温超导研究。赵忠贤院士获得2016年度国家最高科学技术奖。

(1)汞位于第六周期,且与锌同族,写出Hg的最外层电子排布式________。
(2)Ge元素属于_____(从下列选项中选择)
A.s区 B.类金属 C.非金属 D.过渡金属 E.准金属
(3)Ge(CH3)2Cl2分子的中心原子Ge的杂化方式是________
(4)NH3也常作制冷剂,其分子构型是______,NH3的沸点(239.6℃)高于N2沸点的主要原因是_____
(5)图示材料的理想化学式(无空位时)为_____,若Y(钇)元素的化合价为+3,则Cu的平均化合价为___
(6)金属铜为立方晶胞,空间利用率为74%,晶胞边长为a cm,铜的相对原子质量为63.5,阿伏伽德罗常数为NA。则金属铜的晶体密度ρ=_____g/cm3(只含一个系数,用a、NA表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com