
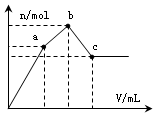
 浓度为 0.1mol•L-1硫酸铝铵[NH4Al(SO4)2]溶液100mL中,逐滴滴入0.1mol•L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )
浓度为 0.1mol•L-1硫酸铝铵[NH4Al(SO4)2]溶液100mL中,逐滴滴入0.1mol•L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )| A. | a点对应的沉淀,其物质的量为0.01mol | |
| B. | b点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-═Al(OH)3↓+2BaSO4↓ | |
| C. | 沉淀质量最大值为4.66g | |
| D. | c点加入Ba(OH)2溶液的体积为250 mL |
分析 100mL 0.1mol•L-1硫酸铝铵[NH4Al(SO4)2],NH4Al(SO4)2物质的量为0.01mol.溶液含有NH4+0.01mol,Al3+0.01mol,SO42-0.02mol.
关键弄清楚反应顺序,开始滴加同时发生反应为SO42-+Ba2+=BaSO4↓,Al3++3OH-=Al(OH)3↓,当Al3+沉淀完全时需加入0.03molOH-,即加入0.015molBa(OH)2,加入的Ba2+为0.015mol,SO42-未完全沉淀,此时溶液含有硫酸铵(开始到a);再滴加Ba(OH)2,生成BaSO4沉淀,发生反应为SO42-+Ba2+=BaSO4↓,NH4++OH-=NH3?H2O,所以沉淀质量继续增加;当SO42-完全沉淀时,共需加入0.02molBa(OH)2,加入0.04molOH-,Al3+反应掉0.03molOH-,生成Al(OH)30.01mol,剩余0.01molOH-恰好与NH4+完全反应,此时溶液中NH4+完全反应,此时溶液为氨水溶液(a到b);继续滴加Ba(OH)2,Al(OH)3溶解,发生反应Al(OH)3+OH-=AlO2-+2H2O,由方程式可知要使0.01molAl(OH)3完全溶解,需再加入0.005molBa(OH)2,此时溶液为氨水与偏铝酸钡溶液(b到c).
解答 解:100mL 0.1mol•L-1硫酸铝铵[NH4Al(SO4)2],NH4Al(SO4)2物质的量为0.01mol.溶液含有NH4+0.01mol,Al3+0.01mol,SO42-0.02mol.
关键弄清楚反应顺序,开始滴加同时发生反应为SO42-+Ba2+=BaSO4↓,Al3++3OH-=Al(OH)3↓,当Al3+沉淀完全时需加入0.03molOH-,即加入0.015molBa(OH)2,加入的Ba2+为0.015mol,SO42-未完全沉淀,此时溶液含有硫酸铵;再滴加Ba(OH)2,生成BaSO4沉淀,发生反应为SO42-+Ba2+=BaSO4↓,NH4++OH-=NH3?H2O,所以沉淀质量继续增加,但增加幅度较前一过程小;当SO42-完全沉淀时,共需加入0.02molBa(OH)2,加入0.04molOH-,Al3+反应掉0.03molOH-,生成Al(OH)30.01mol,剩余0.01molOH-恰好与NH4+完全反应,此时溶液中NH4+完全反应,此时溶液为氨水溶液,沉淀达最大为BaSO4和Al(OH)3;继续滴加Ba(OH)2,Al(OH)3溶解,发生反应Al(OH)3+OH-=AlO2-+2H2O,由方程式可知要使0.01molAl(OH)3完全溶解,需再加入0.005molBa(OH)2,此时溶液为氨水与偏铝酸钡溶液.
A.由分析可知,从开始到a点,发生反应为SO42-+Ba2+=BaSO4↓,Al3++3OH-=Al(OH)3↓,a点对应的沉淀为BaSO4和Al(OH)3,故无法计算沉淀量,故A错误;
B.由分析可知,b点发生反应为SO42-+Ba2+=BaSO4↓,NH4++OH-=NH3?H2O,故总反应方程式为NH4++OH-+SO42-+Ba2+=BaSO4↓+NH3?H2O,故B错误;
C.m=m(BaSO4)+m(Al(OH)3),根据元素守恒得m=n(SO42-)×233g/mol+n(Al3+)×78g/mol=0.02mol×233g/mol+0.01mol×78g/mol=5.44g,故沉淀质量最大值为5.44g,故C错误;
D.由分析可知,c点加入Ba(OH)2的物质的量为0.005mol+0.02mol=0.025mol,所以$\frac{0.025mol}{0.1mol/L}$=0.25L=250ml,故D正确.
故选:D.
点评 本题考查铝化合物的性质及计算,难度比较大,清楚整个反应过程是解题的关键,注意NH4+与Al3+同时存在,OH-首先与Al3+反应,而NH4+与Al(OH)3同时存在,OH-首先与NH4+反应.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:多选题
| 编号 | 实验操作 | 实验目的或结论 |
| A | 将SO2气体通入紫色石蕊试液中,观察溶液是否褪色 | 证明SO2有漂白性 |
| B | 向试管中加入等体积的0.005mol/L的FeCl3溶液和0.01mol/L的KSCN溶液,再滴加几滴饱和FeCl3溶液,观察颜色变化 | 探究增大反应物浓度时平衡移动的方向 |
| C | 将装有NO2和N2O4气体的联通球,一个置于冰水中,一个置于热水中,观察颜色变化 | 探究温度对化学平衡的影响 |
| D | 向硫酸铝溶液中滴加过量的氢氧化钡溶液 产生白色沉淀 | 证明氢氧化铝不溶于过量的氢氧化钡溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
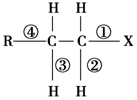
| A. | 发生水解反应时,被破坏的键是④ | |
| B. | 发生消去反应时,被破坏的键是①和② | |
| C. | 发生水解反应时,被破坏的键是①和④ | |
| D. | 发生消去反应时,被破坏的键是①和③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HClO是弱酸,所以NaClO是弱电解质 | |
| B. | Cl2具有很强的氧化性,在化学反应中只能作氧化剂 | |
| C. | 1.12 L Cl2含有1.7NA个质子(NA 表示阿伏加德罗常数) | |
| D. | 过量的铁粉与氯气反应生成FeCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2、O3 | B. | H、D、T | ||
| C. | ${\;}_{19}^{40}$K、${\;}_{20}^{40}$Ca | D. | Na2O、Na2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9:3:1 | B. | 3:2:1 | C. | 6:3:1 | D. | 9:4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定有KNO3,一定没有Na2CO3 | B. | 肯定没有Ba(NO3)2和KNO3 | ||
| C. | 肯定没有Ba(NO3)2,可能有Na2CO3 | D. | 肯定没有Ba(NO3)2,肯定有Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将SO2通入溴水中,溴水褪色证明SO2具有漂白性 | |
| B. | 将含有少量HCl的Cl2通入水中以除去HCl杂质 | |
| C. | 将乙烯通入酸性KMnO4溶液中,溶液褪色证明乙烯具有还原性 | |
| D. | 将蔗糖溶液和少量稀H2SO4混合加热后,加入新制的Cu(OH)2检验蔗糖是否水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
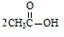 $\stackrel{P_{2}O_{5}}{→}$
$\stackrel{P_{2}O_{5}}{→}$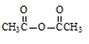 .化合物
.化合物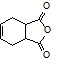 是合成抗病毒药阿昔洛韦的中间体,请设计合理方案以
是合成抗病毒药阿昔洛韦的中间体,请设计合理方案以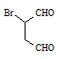 和
和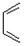 为原料合成该化合物(用合成路线流程图表示,并注明反应条件).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2$\stackrel{Br_{2}}{→}$
为原料合成该化合物(用合成路线流程图表示,并注明反应条件).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2$\stackrel{Br_{2}}{→}$ 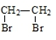
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com