
淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去):实验过程如下:
① 将1∶1的淀粉水乳液与少许硫酸(98%)加入烧杯中,水浴加热至85℃~90℃,保持30 min,然后逐渐将温度降至60℃左右;
② 将一定量的淀粉水解液加入三颈烧瓶中;
③ 控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液;
④ 反应3h左右,冷却,减压过滤后得草酸晶体粗品,再重结晶得草酸晶体。
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
请回答下列问题:
(1)实验①加入98%硫酸少许的目的是: 。
(2)冷凝水的进口是 (填a或b);实验中若混酸滴加过快,将导致草酸产量下降,其原因是 。
(3)装置B的作用是 。为使尾气充分吸收,C中试剂是 。
(4)重结晶时,将草酸晶体粗品经①加热溶解、②趁热过滤、③冷却结晶、④过滤洗涤⑤干燥等实验步骤,得到较纯净的草酸晶体。该过程中可将粗品中溶解度较大的杂质在 (填上述步骤序号)时除去;而粗品中溶解度较小的杂质最后留存在 (填“滤纸上”或“滤液中”)。
(5)将产品在恒温箱内约90℃以下烘干至恒重,得到二水合草酸。用KMnO4标准溶液滴定,该反应的离子方程式为:
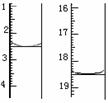 称取该样品0.1200 g,加适量水完全溶解,然后用0.02000 mol·L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图所示,则该草酸晶体样品中二水合草酸的质量分数为 。
称取该样品0.1200 g,加适量水完全溶解,然后用0.02000 mol·L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图所示,则该草酸晶体样品中二水合草酸的质量分数为 。
科目:高中化学 来源: 题型:
对①乙醇②淀粉③油脂④蛋白质的说法,不正确的是
A.等质量的②和③在人体内充分消化吸收时,③释放的能量更大
B.①能使④失去生理活性而变性
C.①可由②水解的最终产物反应制得
D.③和④在人体内的最终代谢产物相同
查看答案和解析>>
科目:高中化学 来源: 题型:
由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流程示意图如下:

(1)在反射炉中,把铜精矿砂和石英砂混合加热到l000℃左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物。该过程中两个主要反应的化学方程式分别是__________、__________,反射炉内生成炉渣的主要成分是__________;
 (2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1200℃左右吹入空气进行吹炼。冰铜中的Cu2S被氧化为Cu2O。生成的Cu2O与Cu2S反应,生成含Cu量约为98. 5%的粗铜,该过程发生反应的化学方程式分别是__________、__________。
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1200℃左右吹入空气进行吹炼。冰铜中的Cu2S被氧化为Cu2O。生成的Cu2O与Cu2S反应,生成含Cu量约为98. 5%的粗铜,该过程发生反应的化学方程式分别是__________、__________。
(3)粗铜的电解精炼如右图所示。在粗铜的电解过程中,粗铜板应是图中电极_____(填图中的字母);在电极d上发生的电极反应式为____________;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期原子序数依次增大的主族元素R、T、Q、W、Y具有如下信息:① R、Y原子的最外层电子数与电子层数相同;② Q是地壳中含量最高的元素,R与T的核电荷数之和等于Q的核电荷数;③ W与R同主族。下列说法正确的是
A.元素Q与W形成的两种常见化合物中含有相同比例的阴、阳离子,属于同种晶体类型
B.元素T、Q、W、Y的原子半径大小为:T<Q<Y<W
C.Q与Y组成的常见物质是一种两性物质,结构中含有共价键
D.由Y和T组成的物质YT是原子晶体,在电子和陶瓷工业上有广泛应用,可以直接由单质Y和T在低温下合成
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.直馏汽油和裂化汽油中分别加入溴的四氯化碳溶液均能发生反应
B.有机物中一定含有C、H元素,可能含有氧、氮元素及卤素等
C.煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来
D.石油主要含有C、H两种元素,石油分馏得到的各馏分均是混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
在乙酸乙酯、乙醇、乙酸水溶液中共存的化学平衡体系中加入含重氢的水,经过足够长的时间后,可以发现,除了水外,体系中含有重氢的化合物是
A.只有乙酸 B.只有乙醇和乙酸
C.只有乙酸和乙酸乙酯 D.乙酸乙酯、乙醇、乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
根据图示填空:

(1)化合物A中含有的官能团是 。
(2)1 mol A与2 mol H2反应生成1 mol E,其反应的化学方程式是 。
(3)与A具有相同官能团的A的同分异构体的结构简式是 。
(4)B经酸化后,与Br2反应得到D,D的结构简式是 。
(5)F的结构简式是 ,由E生成F的反应类型是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.分子式为C5H10的烃,属于烯烃和环烷烃的同分异构体(不包括顺反异构)的种类分别为5,4 B. 分子式为C28H52的烯烃,分子中含有C=C双键的数目是4(不含环状结构)
C.分子式为C3H5Cl的链状化合物(考虑顺反异构)的同分异构体共有3种
D. 分子式为C3H6的有机物最多存在3个C—C单键,与C4H10的碳碳单键数相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com