

(1)用化学方程式表示甲、乙、丙三个工厂合成尿素的原料气H2和CO2的生产过程。
①甲厂以焦炭、空气和水为原料。
②乙厂以天然气、空气和水为原料。
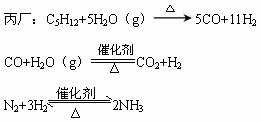
③丙厂以石脑油(主要成分C5H12)、空气和水为原料。
(2)按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算为H2的物质的量)和CO2物质的量之比,则对原料的利用率最高。据此判断甲、乙、丙三个工厂哪个工厂对原料的利用率最高。
解析:绿色化学的最大特点在于它是在始端就采用预防实际污染的科学手段,因而过程和终端均为零排放和零污染。通过化学转化获取新物质的过程中,就是要充分利用每种原料的原子具有“原子经济性”。只有这样,才能做到既充分利用了资源,又实现了防止污染。
答案:

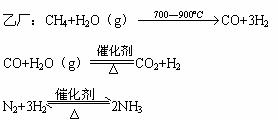
(2)由甲厂生产过程中的化学方程式可得如下关系式:
C+2H2O(g)====2H2+CO2,
得n(H2)∶n(CO2)=2∶1。
由乙厂生产过程中的化学方程式可得如下关系式:
CH4+2H2O(g)![]() 4H2+CO2,
4H2+CO2,
得n(H2)∶n(CO2)=4∶1。
由丙厂生产过程中的化学方程式可得如下关系式:
C5H12(g)+10H2O(g)![]() 16H2+5CO2
16H2+5CO2
得n(H2)∶n(CO2)=16∶5=3.3∶1
由合成CO(NH2)2反应方程式:
2NH3+CO2====CO(NH2)2+H2O
![]()
故对照甲、乙、丙三厂原料气H2和CO2物质的量之比,只有丙厂原料气n(H2)∶n(CO2)=3.3∶1,最接近3∶1,故丙厂对原料利用率最高。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

(1)用化学方程式表示甲、乙、丙三个工厂合成尿素的原料气H2和CO2的生产过程。
①甲厂以焦炭、空气和水为原料;
②乙厂以天然气、空气和水为原料;
③丙厂以石脑油(主要成分为C5H12)、空气和水为原料。
(2)按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算为H2的物质的量)和CO2物质的量之比,则对原料的利用率最高。据此判断哪个工厂对原料的利用率最高。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com