
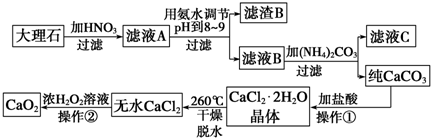
���� ����ʯ����Ҫ�������������������ᷴӦ��������ƺ�������������ҺA�ijɷ�������ƺ��������Լ�ʣ������ᣬ��pH��8-9��Χ����ʱ�������������γɳ�������������B��������������ҺB������ƣ���̼���֮����Է������ֽⷴӦ����̼��ƺ�����泥����ˣ�����̼����������ܽ�Ȼ�������ᾧ���Եõ��Ȼ��ƾ��壬��ʧˮ��Ϊ��ˮ�Ȼ��ƣ�˫��ˮ���Ժ��Ȼ��Ʒ�Ӧ���ɹ������ƺ����ᣬ
��1��ʵ�ֹ����Һ��ķ�����ù��˵ķ��������Ȼ��Ƶ���Һ�л���Ȼ��ƵĽᾧˮ����Ҫ���������ᾧ�ķ�����̼����ܺ�ǿ�ᷴӦ��
��2��pH��8-9��Χ����ʱ�������������γɳ�����
��3�������ܶȻ����������ʱ�������Ѷȼ�С�����жϣ�
��4���ữ����Һ�У�笠�����ˮ�⣻
��5��˫��ˮ���Ժ��Ȼ��Ʒ�Ӧ���ɹ������ƺ��������������Һ��������ᷴӦ�ٽ�ƽ������������ɹ������ƣ�
��6��m g����ʯ��̼��Ƶ����ʵ���Ϊ$\frac{ma}{100}$mol��n g CaO2�����ʵ���Ϊ$\frac{n}{72}$mol������Caԭ�ӵ�������=$\frac{CaO{\;}_{2}�����ʵ���}{CaCO{\;}_{3}�����ʵ���}$��100%���㣮
��� �⣺����ͼʾ��Ϣ���ɵó�����ҺA�ijɷ�������ƺ��������Լ�ʣ������ᣬ��pH��8-9��Χ����ʱ�������������γɳ�������������B��������������ҺB������ƣ���̼���֮����Է������ֽⷴӦ����̼��ƺ�����泥����ˣ�����̼����������ܽ�Ȼ�������ᾧ���Եõ��Ȼ��ƾ��壬��ʧˮ��Ϊ��ˮ�Ȼ��ƣ�˫��ˮ���Ժ��Ȼ��Ʒ�Ӧ���ɹ������ƺ����ᣮ
��1��̼��ƺ�����淋Ļ������˺����ó���̼����������ܽ�Ȼ�������ᾧ���Եõ��Ȼ��ƾ��壬CaCO3 ��ϡ���ᷴӦ��ʵ���ǣ�CaCO3+2H+=Ca2++CO2��+H2O��
�ʴ�Ϊ��A��B��E��
��2���ð�ˮ����pH��8-9�������������γɳ������Ӷ�������������Һ���ʴ�Ϊ����ȥFe3+��
��3���������ҺC��c��CO32-��=10-3��mol/L��Ksp��CaCO3��=4.96��10-9��Ksp=Ca2++CO32-=10-3��mol/L��c��Ca2+��=4.96��10-9 ��c��Ca2+��=4.96��10-6 mol/L����֪c��Ca2+����10-5mol/L����Ϊ������ȫ�����Դ�ʱ�����ӳ�����ȫ��
�ʴ�Ϊ���ǣ�
��4��������ҺC�У�����HNO3ʹ��Һ�������Եõ�������NH4NO3��笠�����ˮ�⣬���ữ����Һ��c��NH4+����c��NO3-����
�ʴ�Ϊ������
��5��˫��ˮ���Ժ��Ȼ��Ʒ�Ӧ���ɹ������ƺ����ᣬ��CaCl2+H2O2=CaO2��+2HCl������NaOH��Һʹ����ƽ��������Ӧ����������CaO2���������ɣ�
�ʴ�Ϊ��CaCl2+H2O2=CaO2��+2HCl������NaOH��Һʹ����ƽ��������Ӧ����������CaO2���������ɣ�
��6��m g����ʯ��̼��Ƶ����ʵ���Ϊ$\frac{ma}{100}$mol��n g CaO2�����ʵ���Ϊ$\frac{n}{72}$mol������Caԭ�ӵ�������=$\frac{CaO{\;}_{2}�����ʵ���}{CaCO{\;}_{3}�����ʵ���}$��100%=$\frac{25n}{18am}$��100%��
�ʴ�Ϊ��$\frac{25n}{18am}$��100%��
���� ���⿼�����Ʊ���������ƣ���Ŀ�Ѷ��еȣ���ȷ�Ʊ�����Ϊ���ؼ���ע�������������ܽ�ƽ�⼰����ת����Ӧ�÷������������������ѧ���ķ�����������ѧʵ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH4�ı���ģ�ͣ�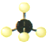 | B�� | �Ҵ��Ľṹ��ʽC2H6O | ||
| C�� | ��Ȳ����ʽ��HC��CH | D�� | ����ļ���ʽ��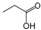 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
| T | �������������ڲ����������4 |
| X | �����������Ǵ�����������2�� |
| Y | �����γɵ���̬�������ڱ�״���µ��ܶ�Ϊ0.76g•L-1 |
| Z | Ԫ����������븺�۵ľ���ֵ֮����6 |
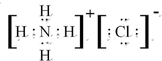 ��
��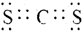 ��
�� ��
��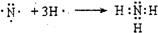 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����һ�գ���ˮ�����գ���ȡ֭�����ù����Ƕ�����ص���ȡ�����ڻ�ѧ�仯 | |
| B�� | ��Ư����Һ�еμ��������ᣬƯ�����ʻ�ӿ� | |
| C�� | �������﷽���ѳ�������ˮ�еĵ����ף��ɷ�ֹˮ�帻Ӫ���� | |
| D�� | �й��Ŵ�����������Һ���������ͭ�������ͭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
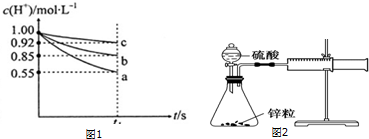
| ��� | �����ϡ����Ũ�� | ��Ӧʱ��/min | �ռ�������/mL | ��Ӧ����mL•min-1 |
| �� | 1mol•L-1 | 11 | 10 | |
| �� | 2mol•L-1 | a | 10 | b |
| �� | 4mol•L-1 | 10 | 5.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
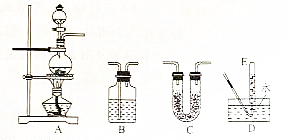
| ѡ�õ����� | ������Լ� |
| A | �������̡�Ũ���ᡢʳ�� |
| B | ����ʳ��ˮ |
| B | KBr��Һ��CCl4�Ļ��Һ |
| D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
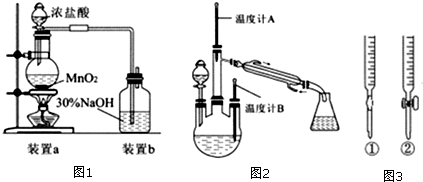
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʱ���ܷ�Ӧ�ǣ�2H2+O2=2H2O | |
| B�� | ����Ϊ����Ⱦ��ˮ�����ڻ����Ѻõ�� | |
| C�� | ȼ�ϵ�ص�����ת�������ﵽ100% | |
| D�� | H2�ڸ���������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com