
| A. | 标准状况下,22.4L CHCl3含氯原子数为3NA | |
| B. | 100mL 1 mol•L-1醋酸溶液中的氢原子数为0.4NA | |
| C. | 常温常压下,11.2g乙烯中共用电子对数为2.4NA | |
| D. | 6.4 g CaC2晶体中所含的离子总数为0.3NA |
分析 A.标准状况下,CHCl3不是气体;
B.醋酸在水中发生电离生成氢离子;
C.根据乙烯的结构计算出含有的共用电子对数目;
D.CaC2晶体中含有阴离子为C22-,阳离子为Ca2+.
解答 解:A.标准状况下,CHCl3不是气体,因此无法计算22.4L CHCl3含氯原子数,故A错误;
B.100mL 1 mol•L-1醋酸溶液中溶质的物质的量为0.1mol,醋酸在水中发生电离生成氢离子,因此氢原子数小于0.4NA,故B错误;
C.11.2g乙烯的物质的量为:$\frac{11.2g}{28g/mol}$=0.4molmol,含有1.6mol碳氢键和0.4mol碳碳键,总共含有2.4mol共用电子对,含有共用电子对数目为2.4NA,故C正确;
D.CaC2晶体的物质的量为$\frac{6.4g}{64g/mol}$=0.1mol,晶体中含有阴离子为C22-,阳离子为Ca2+,则晶体中含有阴阳离子总数为0.2NA,故D错误;
故选C.
点评 本题考查了考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意标准状况下CHCl3的状态不是气体,阿伏加德罗常数是历年高考的“热点”问题,这是由于它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容.


科目:高中化学 来源: 题型:解答题
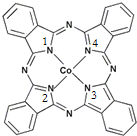 钴(Co)是人体必需的微量元素.含钴化合物作为颜料,具有悠久的历史,在机械制造、磁性材料等领域也具有广泛的应用.请回答下列问题:
钴(Co)是人体必需的微量元素.含钴化合物作为颜料,具有悠久的历史,在机械制造、磁性材料等领域也具有广泛的应用.请回答下列问题: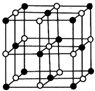 ,在该晶体中与一个钴原子等距离且最近的钴原子有12个;筑波材料科学国家实验室一个科研小组发现了在 5K 下呈现超导性的晶体,该晶体具有CoO2的层状结构(如下图所示,小球表示Co原子,大球表示O原子).下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是D.
,在该晶体中与一个钴原子等距离且最近的钴原子有12个;筑波材料科学国家实验室一个科研小组发现了在 5K 下呈现超导性的晶体,该晶体具有CoO2的层状结构(如下图所示,小球表示Co原子,大球表示O原子).下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是D.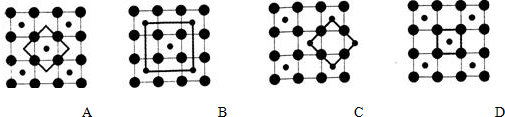
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
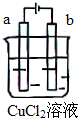
| A. | 电极a表面呈红色 | |
| B. | 电极b表面有气泡生成 | |
| C. | 电子由电源的负极沿导线流向电极b | |
| D. | 该装置能量转化形式为化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.4mol/L | B. | 0.2mol/L | C. | 0.1mol/L | D. | 0.08mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①②③均属于氧化还原反应 | B. | H2和HCl均可循环利用 | ||
| C. | SiO2是一种坚硬难熔的固体 | D. | 硅可用于制作光导纤维 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com