
氢化亚铜(CuH)是一难溶物质,用CuSO4溶液和另一种“反应物”在40~50 ℃时反应可生成它。CuH不稳定,易分解;CuH在氯气中能燃烧,跟盐酸反应能产生气体。下列有关推断中错误的是 ( )
A.这里的“另一种反应物”具有还原性
B.CuH可作氧化剂、还原剂
C.CuH+Cl2===CuCl+HCl(燃烧)
D.CuH+HCl===CuCl+H2↑(常温)
 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
水是一种重要的自然资源,是人类赖以生存不可缺少的物质。水的处理主要包括水的净
化、污水处理、硬水软化和海水的淡化等。
(1)海水的淡化常用的方法有_________、
_________、电渗析法等。
(2)电渗析法是近年来发展起来的一种较好
 的海水淡化技术,其原理如图所示。
的海水淡化技术,其原理如图所示。
①阳极(惰性电极)的电极反应式为 __________________.
②淡水的出口为a、b、c中的_________ 出口。
③某出口排出的浓海水中溴元素的含量为0.68g/L,现用氯气将其中的溴离子
氧化为溴单质,则处理l.Ox10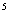 L该浓海水需标况下的氯气的体积为_________
L该浓海水需标况下的氯气的体积为_________ 。
。
(3) K2FeO4是自来水厂常用的消毒、净化剂。工业上常用Fe(NO3)3溶液与浓KCIO溶液在强碱性环境中生成K2FeO4,该反应的离子方程式为___________________________.
(4)氯碱工业常用_________(填“阴”或“阳”)离子交换膜电解槽电解精制的饱和食盐水, 若食盐水中含有杂质MgCl2则会对离子交换膜电解槽造成损害,其原因是_______ (用离子方程式表示)。
(5)工程塑料ABS合成时,用了以下三种单体: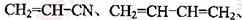 、
、
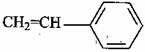 ,请写出ABS的结构简式_______________________________。
,请写出ABS的结构简式_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,一定量的A和B气体发生如下可逆反应: A(g)+3B(g)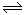 3C(g),只有反应到达平衡时才具有的性质是 ( )
3C(g),只有反应到达平衡时才具有的性质是 ( )
A. 各物质的浓度之比为1:3:3 B.反应后混合物中各物质的量浓度相等
C. A、B、C三种物质的浓度不随时间变化而变化 D. ν(A)、ν(B)、ν(C) 之比为1:3:3
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学设计了如下实验测量m g铜银合金样品中铜的质量分数:

下列说法中不正确的是 ( )
A.合金的熔点比其成分金属低,通常比成分金属具有更优良的金属特性
B.铜银都能与稀硝酸反应,收集到的V L气体可能全为NO
C.操作Ⅰ是过滤,操作Ⅱ是洗涤,操作Ⅲ应是烘干
D.根据反应收集到的气体体积可以计算铜和银的质量分数
查看答案和解析>>
科目:高中化学 来源: 题型:
信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70% Cu、25% Al、4% Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
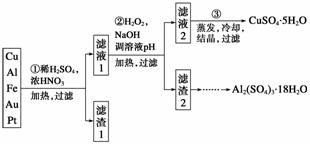
请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为_______________________________________
________________________________________________________________________;
得到滤渣1的主要成分为____________。
(2)第②步加H2O2的作用是______________,使用H2O2的优点是______________;调溶液pH的目的是使______________生成沉淀。
(3)用第③步所得CuSO4·5H2O制备无水CuSO4的方法是________________________。
(4)由滤渣2制取Al2(SO4)3·18H2O ,探究小组设计了三种方案:
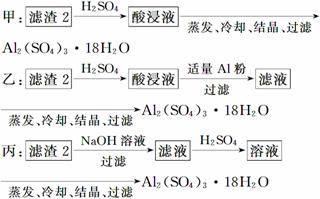
上述三种方案中,________方案不可行,原因是_______________________________
________________________________________________________________________;
从原子利用率角度考虑,__________方案更合理。
查看答案和解析>>
科目:高中化学 来源: 题型:
铜有两种常见的氧化物CuO和Cu2O。某学习小组取0.98 g(用精密天平测量)Cu(OH)2固体,将其加热有铜的氧化物生成,其质量随温度变化的曲线如图1所示。

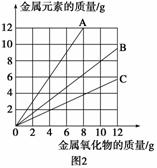
另外,某同学绘制了三条表示金属氧化物与其所含金属元素质量的关系曲线,如图2所示。则下列分析正确的是 ( )
A.图1中产物a、b的化学式分别为Cu2O和CuO
B.图1整个过程中共生成0.26 g H2O
C.图2三条曲线中,表示CuO和其中所含Cu元素质量的关系曲线是曲线A
D.图2中绘制错误的曲线共2条
查看答案和解析>>
科目:高中化学 来源: 题型:
在25 ℃时,FeS的Ksp=6.3×10-18,CuS的Ksp=1.3×10-36,ZnS的Ksp=1.3×10-24。下列有关说法中正确的是( )
A.25 ℃时,CuS的溶解度大于ZnS的溶解度
B.25 ℃时,饱和CuS溶液中Cu2+的浓度为1.3×10-36 mol·L-1
C.物质的量浓度相同的FeCl2、ZnCl2混合液中加入少量Na2S,只有FeS沉淀生成
D.除去某溶液中的Cu2+,可以选用FeS作沉淀剂
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E均为易溶于水的化合物,其离子组成如下。(各化合物中离子组成不重复)
| 阳离子 | Na+、Al3+、Ag+、Ba2+、Fe3+ |
| 阴离子 | Cl-、CO |
分别取溶液进行如下实验:
①用pH试纸分别测得B、C溶液均呈碱性,且0.1 mol/L B溶液pH>13;
②D溶液加入铜粉,溶液质量增加;
③在E溶液中加过量B,没有沉淀产生;
④在A溶液中逐滴滴入氨水至过量,先先成白色沉淀,后沉淀溶解。
请回答下列问题:
(1)B的名称:________,E的名称:________。
(2)C水溶液呈碱性的原因(用离子方程式表示):________;0.1 mol/L的C溶液中和0.1 mol/L的NaHCO3溶液中,阴离子的总数:C溶液________NaHCO3溶液。(填“>”、“=”或“<”)
(3)D溶液呈________(填“酸性”、“碱性”或“中性”);若将D溶液加热蒸干,得到的固体应是:________________________。(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
莽草酸是合成治疗禽流感的药物——达菲(Tamiflu)的原料之一。莽草酸是A的一种异构体。A的结构简式如下:
ഠ
(1)A的分子式是 。
(2)A与溴的四氯化碳溶液反应生成物的结构简式是
(3)A与氢氧化钠溶液反应的化学方程式(有机物用结构简式表示)是
(4)17.4克A与足量碳酸氢钠溶液反应,计算生成二氧化碳的体积 (标准状况)。(5)A在浓硫酸作用下加热可得到B(B的结构简式为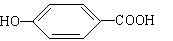 ),其反应类型 。
),其反应类型 。
(6)B的同分异构体中既含有酚羟基又含有酯基的共有 种,写出其中一种同分异构体的结构简式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com