
分析 (1)金属性越强,与酸反应越剧烈;
(2)根据电子转移守恒,金属提供电子越多,相同条件下生成氢气越多;
(3)根据电子转移守恒,相同条件下,生成氢气体积之比等于金属提供电子之比.
解答 解:(1)金属性Na>Mg>Al,故Na与酸反应剧烈程度最大,故答案为:Na;
(2)物质的量相等的Na、Mg、Al与盐酸反应中Al提供电子最多,根据电子转移守恒,相同条件下Al与盐酸反应生成氢气最多,故答案为:Al;
(3)物质的量相等的Na、Mg、Al与盐酸反应中提供电子数目之比为1:2:3,根据电子转移守恒,相同条件下,生成氢气体积之比为1:2:3,故答案为:1:2:3.
点评 本题考查化学方程式计算,侧重考查学生分析计算能力,注意利用电子转移守恒解答,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 能全部透过半透膜 | B. | 能全部通过滤纸 | ||
| C. | 粒子做布朗运动 | D. | 有电泳现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间 (s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/10-4mol/L | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)/10-3mol/L | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
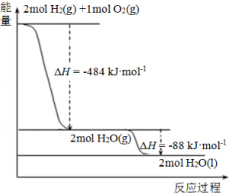
| A. | 926 kJ•mol-1 | B. | 485kJ•mol-1 | C. | 463 kJ•mol-1 | D. | 221 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com