
| A. | 在一定温度,相同浓度时电离平衡常数(K)越大可以表示弱电解质电离程度越大 | |
| B. | 电离平衡常数(K)与温度无关 | |
| C. | 不同浓度的同一弱电解质,其电离平衡常数(K)不同 | |
| D. | 多元弱酸各步电离平衡常数相互关系为K1<K2<K3 |
分析 A.温度一定时,电离平衡常数越大,说明该物质越容易电离;
B.电离平衡常数只与温度有关;
C.同一电解质的电离平衡常数只与温度有关,与溶液浓度无关;
D.多元弱酸电离平衡常数中,其电离程度依次减小.
解答 解:A.温度一定时,电离平衡常数越大,说明该物质越容易电离,即其电离程度越大,故A正确;
B.电离平衡常数只与温度有关,与溶液酸碱性及浓度无关,故B错误;
C.同一电解质的电离平衡常数只与温度有关,与溶液浓度无关,所以同一物质在相同温度下的电离平衡常数相同,故C错误;
D.多元弱酸电离平衡常数中,因为前边电离出的氢离子抑制后边电离,所以其电离程度依次减小,故D错误;
故选A.
点评 本题考查弱电解质的电离,为高频考点,侧重考查学生对电离平衡常数概念的理解,电离平衡常数只与温度有关,与溶液浓度及溶液导电性强弱无关,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | K2CO3:CO${\;}_{3}^{2-}$+2H20?H2CO3+OH- | B. | Ca(ClO)2:ClO-+H2O=HClO+OH- | ||
| C. | Ba(HCO3)2:HCO3-+H2O?H3O++CO32- | D. | Na2SO3:SO32-+H2O?HSO3-+OH- |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高一上第一次月考化学卷(解析版) 题型:选择题
配制一定物质的量浓度的NaCl溶液时,导致浓度偏高的原因可能是
A. 移液时,不慎将液体流到瓶外
B. 容量瓶中原有少量的蒸馏水
C. 容量瓶盛过Na2CO3溶液,使用前未洗涤
D. 定容时读数仰视
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液的pH | B. | 醋酸的电离平衡常数 | ||
| C. | 溶液的导电能力 | D. | 醋酸的电离程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸 | HClO2 | HF | HCN | H2S |
| Ka | 1×10-2 | 6.3×10-4 | 4.9×10-10 | K1=9.1×10-8K2=1.1×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
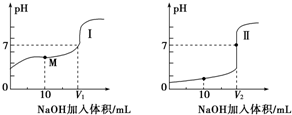
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com