
分析 生成固体2.00g为MgO,还生成水,结合n=$\frac{m}{M}$、n=$\frac{V}{Vm}$及原子守恒计算.
解答 解:n(CO2)=$\frac{0.896L}{22.4L/mol}$=4.00×10-2 mol,
n(MgO)=$\frac{2.00g}{40g/mol}$=5.00×10-2 mol,
n(H2O)=$\frac{4.66g-0.04mol×44g/mol-2.00g}{18g/mol}$=5.00×10-2 mol,
碱式碳酸镁分解生成n(MgO):n(CO2):n(H2O)=(5.00×10-2):(4.00×10-2):(5.00×10-2)=5:4:5,
可知碱式碳酸镁的化学式为Mg(OH)2•4MgCO3•4H2O,
答:碱式碳酸镁的化学式为Mg(OH)2•4MgCO3•4H2O.
点评 本题考查化学反应的计算,为高频考点,把握物质的量的计算、原子守恒为解答的关键,侧重分析与计算能力的考查,注意守恒法的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 蔬菜水果多属于碱性食物,对人体健康有益 | |
| B. | 棉花、合成橡胶都属于合成材料 | |
| C. | 蚕丝、羊毛完全燃烧只生成CO2和H2O | |
| D. | 苯、植物油均能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
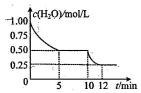 在2L密闭容器中进行反应C(s)+H2O(g)?CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图.下列判断正确是( )
在2L密闭容器中进行反应C(s)+H2O(g)?CO(g)+H2(g)△H>0,测得c(H2O)随反应时间(t)的变化如图.下列判断正确是( )| A. | 0~5min内,v(H2)=0.05mol/(L•min) | |
| B. | 5min时该反应的K值一定小于12min时的K值 | |
| C. | 10min时,改变的外界条件可能是减小压强 | |
| D. | 5min时该反应的v(正)大于11min时的v(逆) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
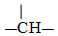 、
、 等结合而成的.试写出同时满足下列条件的烷烃的结构简式:
等结合而成的.试写出同时满足下列条件的烷烃的结构简式: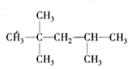
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯(硝基苯) | B. | 乙醇(乙酸) | C. | 乙酸乙酯(乙酸) | D. | 乙酸(苯) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
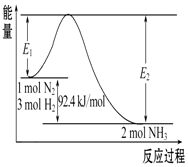 科学家一直致力于“人工固氮”的方法研究.
科学家一直致力于“人工固氮”的方法研究.| t℃ | 473 | 573 | 673 | … |
| K | 4.4×10-2 | K1 | K2 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
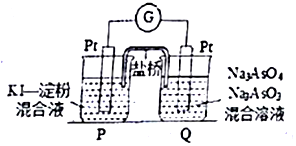 砷(As)是第四周期第VA族元素,用化学用语回答问题.
砷(As)是第四周期第VA族元素,用化学用语回答问题. ,其气态氢化物的稳定性比AsH3强(填“强”或“弱”)
,其气态氢化物的稳定性比AsH3强(填“强”或“弱”)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com