
【题目】下列说法正确的是
A. HS-的水解方程式为:HS-+ H2O![]() H3O++S2-
H3O++S2-
B. CH3COOH 溶液加水稀释后,溶液中![]() 的值减小
的值减小
C. 将pH =4的盐酸稀释后,溶液中所有离子的浓度均降低
D. 100℃时,pH=12的纯碱溶液中:c(OH-)=1.0×10-2 mol·L-1
科目:高中化学 来源: 题型:
【题目】醇酸树脂是一种成膜性好的树脂,下面是一种醇酸树脂的合成线路:

已知:
(1)有机物A中含有的官能团是____________(填汉字);写出B的结构简式是______________;E的分子式为_____________________。
(2)反应①的化学方程式是_________________,属于_______反应。
(3)反应①-④中属于取代反应的是________(填序号)。
(4)反应④的化学方程式为是_______________________。
(5)写出一种符合下列条件的与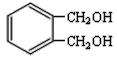 互为同分异构体的结构简式 ______________。
互为同分异构体的结构简式 ______________。
a.能与浓溴水反应生成白色沉淀,
b.通过核磁共振发现,苯环上只有两种不同化学环境的氢,且峰面积比为1∶1,
c.能发生消去反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察法是研究物质性质的一种基本方法。一同学将一小块金属钠露置于空气中,观察到下列现象:银白色![]() 变暗
变暗![]() 变白色
变白色![]() 出现液滴
出现液滴![]() 白色固体粉末。下列说法正确的是( )
白色固体粉末。下列说法正确的是( )
A.银白色变暗是因为生成了过氧化钠
B.出现液滴是因为NaOH具有吸湿性
C.过程④只发生了物理变化
D.最后得到的白色固体是NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,加少量烧碱溶液可使溶液中c(H+)/c(CH3COOH)值增大。
CH3COO-+H+,加少量烧碱溶液可使溶液中c(H+)/c(CH3COOH)值增大。
B. 25 ℃时,向水中加入少量固体CH3COONa,水的电离平衡:H2O![]() H++OH-逆向移动,c(H+)降低
H++OH-逆向移动,c(H+)降低
C. 取c(H+)=0.01 mol·L-1的盐酸和醋酸各100 mL,分别稀释2倍后,再分别加入0.03 g锌粉,在相同条件下充分反应,醋酸与锌反应的速率大
D. 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液中:c(Na+)<c(NO3- )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
弱酸 | HCOOH | HCN | H2CO3 |
电离常数(25℃) | Ka = 1.77×10 -4 | Ka=4.3×l0-10 | Ka1=5.0×l0-7 Ka2=5.6×l0-11 |
①0.1 moI/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)______c(HCO3 -)(填“>”、“<”或“=”)。
②常温下,pH相同的三种溶液
A.HCOONa B.NaCN C.Na2CO3,
其物质的量浓度由大到小的顺序是________(填编号)。
③已知25℃时,HCOOH( aq) +OH -( aq)=HCOO-(aq) +H2O(1) △H=-a kJ/mol
H+(aq) +OH-(aq) =H2O(1) △H=-b kJ/mol
甲酸电离的热化学方程式为__________________________________。
④将少量CO2通入NaCN溶液,反应的离子方程式是______________________。
⑤室温下,—定浓度的HCOONa溶液pH =9,用离子方程式表示溶液呈碱性的原因是:
______________________________,溶液中![]() =___________。
=___________。
(2)室温下,用0.100 mol/L盐酸溶液滴定20.00mL0.l00mol/L 的某氨水溶液,滴定曲线如图所示。

①d点所示的溶液中离子浓度由大到小的顺序依次为_______________。
②b点所示的溶液中c(NH3·H2O)-c(NH4+)=_____(用溶液中的其它离子浓度表示)。
③pH =10的氨水与pH =4的NH4C1溶液中,由水电离出的c(H+)之比为____。
(3)已知Ksp(BaCO3) =2.6×l0-9,Ksp( BaSO4)=1.1×10-10.
①现将浓度为2×10-4mol/LNa2CO3溶液与BaCl2溶液等体积混合,则生成BaCO3沉淀所需BaCl2溶液的最小浓度为____mol/L。
②向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中![]() =___________(保留三位有效数字)。
=___________(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面提到的问题中,与盐的水解有关的是( )
①明矾和FeCl3可作净水剂
②为保存FeCl3溶液,要在溶液中加少量盐酸
③实验室配制AlCl3溶液时,应先把它溶解在盐酸中,而后加水稀释
④NH4Cl溶液可作焊接中的除锈剂
⑤实验室盛放Na2SiO3溶液的试剂瓶应用橡皮塞,而不能用玻璃塞
⑥用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂
⑦在NH4Cl或AlCl3溶液中加入金属镁会生成氢气
⑧草木灰与铵态氮肥不能混合施用
⑨加热蒸干AlCl3溶液得到Al(OH)3固体.
A. ①④⑦ B. ②⑤⑧ C. ③⑥⑨ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中使用的购物袋的材料多为聚乙烯,工农业生产中使用的塑料也是聚乙烯。下列有关说法正确的是( )
A.聚乙烯的单体能够使溴的四氯化碳溶液褪色
B.聚乙烯既可以人工合成,也可以从自然界中获取
C.聚乙烯与乙烯的性质相似
D.用纯净的乙烯合成的聚乙烯是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯和溴取代反应的实验装置如图所示,其中A为由具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉.填写下列空白:
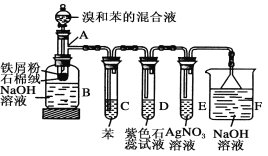
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒内就发生反应.写出A中所发生反应的化学方程式(有机物写结构简式):______________________________.
(2)B中NaOH溶液的作用是______________________________.
(3)试管C中苯的作用是_________________________________.
(4)反应开始后,观察D和E两试管,看到的现象为______________,此现象可以验证苯和液溴的反应为____________(填反应类型).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如下流程:

下列说法不正确的是( )
A. 溶解烧渣选用足量硫酸,试剂X选用铁粉
B. 固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al(OH)3,进入固体2
C. 从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解
D. 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com