
| A、酸a的浓度可能大于b |
| B、酸a的浓度可能等于b |
| C、酸a的酸性比醋酸弱 |
| D、酸a可能是强酸可能是弱酸 |


科目:高中化学 来源: 题型:
| A、将pH=3的醋酸稀释后,溶液中所有离子的浓度均降低 |
| B、在纯水中加入少量NaOH或醋酸钠均可抑制水的电离 |
| C、常温下,将pH=3的盐酸和pH=11的氨水等体积混合,溶液的pH>7 |
| D、用标准NaOH溶液滴定醋酸至刚好完全反应时,溶液中C(Na+)=C(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、未经冷却趁热将溶液注入容量瓶中 |
| B、摇匀后发现液面低于刻度线再加水 |
| C、容量瓶中原有少量蒸馏水 |
| D、定容时仰视观察液面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、68.76kJ |
| B、57.30 kJ |
| C、34.38kJ |
| D、17.19 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2和H2在一定条件下合成氨,可以实现固氮 |
| B、用氨水吸收CO2,可以捕捉碳,降低温室效应 |
| C、对煤炭、石油脱硫,可以减少酸雨 |
| D、PM2.5是指大气中直径接近2.5微米的颗粒物,入肺影响健康.它在空气中为气溶胶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性,回答下列问题:
4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
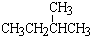 ; ⑧CH3CH2CH2CH3与CH3CH(CH3)2
; ⑧CH3CH2CH2CH3与CH3CH(CH3)2查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com