
下图为几种晶体或晶胞的示意图:

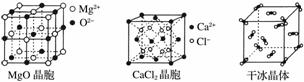
请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成的晶体是________________。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为________________________。
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能________(填“大于”或“小于”)MgO晶体,原因是________________________。
(4)每个Cu晶胞中实际占有________个Cu原子,CaCl2晶体中Ca2+的配位数为________。
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是________________________________。
科目:高中化学 来源: 题型:
下列排列方式中,A.ABCABCABC B.ABABABABAB C.ABBAABBA D.ABCCBAABCCBA,属于镁型堆积方式的是____________;属于铜型堆积方式的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图:
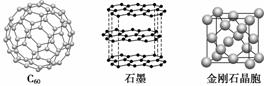
回答下列问题:
(1)金刚石、石墨、C60、碳纳米管等都是碳元素的单质形式,它们互为____________。
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为________、________。
(3)C60属于________晶体,石墨属于________晶体。
(4)石墨晶体中,层内C—C键的键长为142 pm,而金刚石中C—C键的键长为154 pm。其原因是金刚石中只存在C—C间的________共价键,而石墨层内的C—C间不仅存在________共价键,还有________键。
(5)金刚石晶胞含有____________个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r=__________a,列式表示碳原子在晶胞中的空间占有率__________(不要求计算结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.由于铵盐中是有离子键构成的,因而化学性质相当稳定
B.分子晶体中都存在分子间作用力,但可能不存在共价键
C.在常见的四种晶体类型中,都有“原子(离子)半径越大,物质熔点越低”的规律
D.常温下为气态或液态的物质,其固态时一定会形成分子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则ω g R原子完全转化为R2-时,含有电子的物质的量是 ( )
A.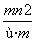 mol B.
mol B. mol
mol
C.ω(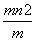 ) mol D.
) mol D.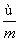 (m-n+2) mol
(m-n+2) mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下图为几种粒子的结构示意图,完成以下填空。
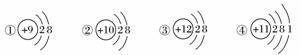
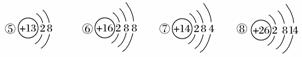
(1)属于阳离子结构的粒子是________(填编号,下同)。
(2)具有稳定性结构的原子是__________________。
(3)只能得电子的粒子是______________;只能失电子的粒子是______________;既能得电子,又能失电子的粒子是____________________________。
(4)③粒子半径________④粒子半径(填“大于”、“小于”或“等于”)。
(5)某元素R形成的氧化物为R2O3,则R的离子结构示意图可能是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
原子数相同、电子总数相同的粒子,互称为等电子体。硼元素可形成三个等电子体阴离子:BO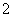 、BC
、BC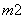 和BN
和BN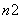 ,则m、n值为( )
,则m、n值为( )
A.5、3 B.2、4 C.3、1 D.1、2
查看答案和解析>>
科目:高中化学 来源: 题型:
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法探究影响化学反应速率的因素。
实验一:利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol·L-1、2 mol·L-1、18.4 mol·L-1),设计实验方案,研究影响反应速率的因素。
(1)甲同学的实验报告如表所示:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取三份等体积的2 mol·L-1 硫酸于试管中 ②分别投入大小、形状相同的 Cu、Fe、Mg | 反应产生气泡的速率大小: Mg>Fe>Cu | 反应物的性质越活泼,反应速 率越大 |
该同学的实验目的是__________________,要想得出正确的实验结论,还需要控制的实验条件是________________________________________________________________________。
(2)乙同学为了能精确地研究浓度对反应速率的影响,在相同温度下利用如图所示装置进行定量实验。完成该实验应选用的实验药品是__________,应该测定的实验数据是________________________________________________________________________。
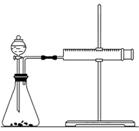
实验二:已知2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在开始一段时间内反应速率较小,溶液褪色不明显,但反应一段时间后,溶液突然褪色,反应速率明显增大。
(3)针对上述实验现象,某同学认为该反应放热,导致溶液的温度升高,从而使反应速率增大。从影响化学反应速率的因素看,你认为还可能是________的影响。
(4)若要用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,还可以在反应开始时加入________(填字母)。
A.硫酸钾 B.硫酸锰
C.氯化锰 D.水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com