
| A. | ③④⑧ | B. | ④⑤⑧ | C. | ③④⑤ | D. | ④⑤⑦⑧ |
分析 既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色,则有机物中含碳碳双键或碳碳三键,以此解答该题.
解答 解:①甲烷与高锰酸钾、溴水均不反应;
②苯与高锰酸钾、溴水均不反应;
③聚乙烯中不含双键,与高锰酸钾、溴水均不反应;
④乙烯中含双键,与高锰酸钾、溴水均反应使其褪色;
⑤2-丁炔中含碳碳三键,与高锰酸钾、溴水均反应使其褪色;
⑥己烷与高锰酸钾、溴水均不反应;
⑦邻二甲苯与溴水不反应;
⑧氯乙烯中含双键,与高锰酸钾、溴水均反应使其褪色,
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、炔烃等有机物及分析与应用能力的考查,题目难度不大.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:实验题
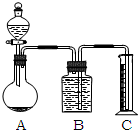 甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验.
甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
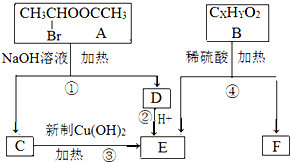 六种有机物之间的转化关系如图.已知:一个碳原子上连有两个羟基的结构极不稳定,易发生变化:R-CH(OH)2→RCHO+H2O
六种有机物之间的转化关系如图.已知:一个碳原子上连有两个羟基的结构极不稳定,易发生变化:R-CH(OH)2→RCHO+H2O
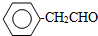 或
或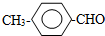 或(邻位、间位).
或(邻位、间位).查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,故溶液pH不变 | |
| B. | 电解稀氢氧化钠溶液要消耗OH-,故溶液pH减小 | |
| C. | 电解硫酸钠溶液,在阴极上发生反应:4OH--4e-═2H2O+O2↑ | |
| D. | 电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 项目 | 物质 | 杂质(少量) | 试剂 | 操作方法 |
| A | CO2 | SO2 | 饱和NaHCO3溶液 | 洗气 |
| B | 硝酸 | 盐酸 | 过量的AgNO3溶液 | 过滤 |
| C | 溴苯 | 溴 | 加入CCl4 | 分液 |
| D | Na2CO3 | Na2SO4 | 加入适量BaCl2溶液 | 溶解、过滤、洗涤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com