
【题目】某学生利用以下装置探究氯气与氨之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨反应的装置。请回答下列问题:

(1)装置A中发生反应的化学方程式为_________________________________;
(2)装置E中盛装的溶液是___________;
(3)装置B能否用装置D替换,原因是____________________________________;
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。写出反应的化学方程式________________________________________,在标准状况下,448 mL NH3参加反应,则转移的电子数为__________。(用NA代表阿伏加德罗常数)
【答案】 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O 饱和食盐水 不能,硫酸与氨气反应 8NH3+3Cl2=6NH4Cl+N2 0.015 NA
CaCl2+2NH3↑+2H2O 饱和食盐水 不能,硫酸与氨气反应 8NH3+3Cl2=6NH4Cl+N2 0.015 NA
【解析】分析:(1)氯化铵和氢氧化钙在加热条件下能反应生成氯化钙、氨气和水;
(2)依据浓盐酸具有挥发性,可知制取的氯气中含有氯化氢、水蒸气,要收集干燥纯净的氯气,应除去氯化氢、水蒸气;
(3)氨气为碱性气体应选择碱性干燥剂;氯气为酸性气体应选择酸性干燥剂;
(4)由题意可知发生反应为氨气和氯气生成氯化铵和氮气,依据原子个数、得失电子守恒写出反应方程式并计算注意电子数。
详解:(1)氯化铵和氢氧化钙在加热条件下能反应生成氯化钙、氨气和水,反应的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
(2)浓盐酸具有挥发性,所以制备的氯气中含有氯化氢和水蒸气,依次通过盛有饱和食盐水洗气瓶E、盛有浓硫酸洗气瓶D可以除去氯化氢和水蒸气,即装置E中盛装的溶液是饱和食盐水;
(3)氨气为碱性气体应选择碱性干燥剂,浓硫酸为酸性干燥剂,能够与氨气反应,不能干燥氨气,因此装置B不能用装置D替换;
(4)氨气和氯气反应生成白烟氯化铵和空气的主要成分之一氮气,反应的化学方程式为8NH3+3Cl2=6NH4Cl+N2;448mL氨气的物质的量是0.448L÷22.4L/mol=0.02mol,反应中每消耗8mol氨气生成1mol氮气,转移6mol电子,所以消耗0.02mol氨气,转移电子是![]() ,个数是0.015 NA。
,个数是0.015 NA。


 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】对下列有机化学的认识中,错误的是
A. 反应 ![]() 属于取代反应
属于取代反应
B. 淀粉和纤维素属于多糖,在人体内水解转化为葡萄糖,为人类提供能量
C. 分枝酸结构简式如图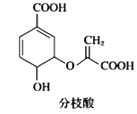 ,可与乙醇、乙酸反应,也可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色
,可与乙醇、乙酸反应,也可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色
D. 取蔗糖水解液少许,先滴加过量的NaOH溶液,再滴入新制的氢氧化铜悬浊液,加热,有红色沉淀生成,证明其水解产物具有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铁及其化合物的说法正确的是( )
A.将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红,可以检验Fe(NO3)2晶体是否已氧化变质
B.浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体
C.1 mol FeI2与足量氯气反应时转移的电子数为2NA
D.水溶液中Fe2+、H+、SO ![]() 、ClO﹣不能大量共存
、ClO﹣不能大量共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知:b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法不正确的是
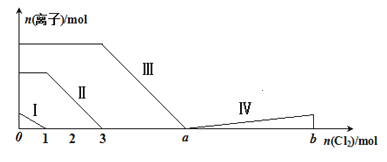
A. 线段Ⅱ表示Fe2+的变化情况
B. 线段Ⅳ发生反应的离子方程式为:I2+5Cl2+12OH-=2IO3-+10Cl-+6H2O
C. 根据图象可计算a=6
D. 原溶液中c(Fe2+)∶c(I-)∶c(Br-)=2∶1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氧化还原反应的叙述,正确的是( )
A.一定有氧元素参加B.还原剂本身发生还原反应
C.氧化剂本身发生氧化反应D.一定有电子转移(得失或偏移)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学常见单质A、B和甲、乙、丙三种化合物有如图所示的转换关系(部分产物未列出).单质A常作为食品包装材料,甲是两性氧化物. 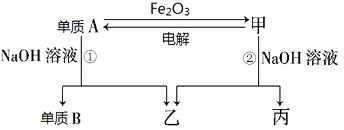
根据图示转化关系回答:
(1)写出下列物质的化学式:单质A , 乙 .
(2)写出单质A与Fe2O3反应的化学方程式: , 利用该反应的原理,可用于
(3)用单质A做成的容器可以储存和运输浓硫酸的原因是 .
(4)写出反应①的离子方程式: .
(5)工业上冶炼下列物质通常 不采用电解法的是 .
a.Na b.Mg c.Fe d.Ag
(6)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有
a.KCl b.KClO 3 c.MnO2 d.Mg.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】龙胆酸酯对体外培养的黑素细胞产生黑素的能力有明显的抑制效应,且没有细胞毒性和诱变力。是—种高效无毒的药物皮肤美白剂。合成龙胆酸烷基酯类路线如下:
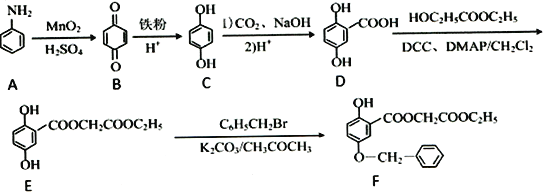
(1)F中含氧官能团的名称为羟基、_____________、_____________。
(2)E→F的反应类型是_______________。
(3)写出D→E反应的化学方程式:_________________________________。
(4)写出满足下列条件的龙胆酸乙酯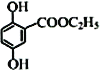 的任意一种同分异构体的结构简式:__________。
的任意一种同分异构体的结构简式:__________。
Ⅰ.能发生银镜反应,与FeCl3不发生显色反应但其水解产物之一能与FeCl3发生显色反应
Ⅱ.核磁共振氢谱有四组峰,且峰面积之比为6 : 2 : 1 : 1
(5)已知: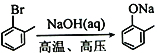 。水杨酸乙酯(
。水杨酸乙酯( )广泛应用于日用香皂等,根据已有知识并结合相关信息,写出以苯、乙醇为原料制备水杨酸乙酯的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)___________________。
)广泛应用于日用香皂等,根据已有知识并结合相关信息,写出以苯、乙醇为原料制备水杨酸乙酯的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com