
【题目】保持洁净安全的生存环境已成为全人类的共识。
(1)某日空气中各种污染物的污染指数分别为:二氧化硫66,二氧化氮50,可吸入颗粒120。该地区的当日首要污染物是 。
(2)汽车尾气(含有烃类、CO、SO2与NO等物质)是城市的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成无毒气体,并促使烃类充分燃烧及SO2的转化。写出CO与NO反应的化学方程式: 。
(3)pH< 的雨水称为酸雨;向煤中加入适量的 ,可以大大减少燃物产物中SO2的量。
(4)1998年我国长江流域发生百年一遇的洪水,洪水泛滥期间为解决灾民的饮用水问题,防疫人员向灾民发放明矾来净化河水。明矾的净水原理是 (用有关反应的离子方程式表示)。
【答案】
(1)可吸入颗粒物;
(2)2NO+2CO![]() N2+2CO2;
N2+2CO2;
(3)5.6;CaCO3(或CaO);
(4)Al3++3H2O![]() Al(OH)3(胶体)+3H+。
Al(OH)3(胶体)+3H+。
【解析】
试题分析:(1)二氧化硫86,二氧化氮71,可吸入颗粒物162,污染指数的数值最大的是可吸入颗粒物,故答案为:可吸入颗粒物;
(2)“催化转换器”使CO与NO反应,生成无毒气体为氮气和二氧化碳,该反应为2NO+2CO![]() N2+2CO2,故答案为:2NO+2CO
N2+2CO2,故答案为:2NO+2CO![]() N2+2CO2;
N2+2CO2;
(3)空气中含有二氧化碳,二氧化碳能和雨水反应生成碳酸,碳酸显酸性,所以正常的雨水常呈微酸性,pH约为5.6;而二氧化硫、氮氧化物是形成酸雨的重要物质,其溶液的pH<5.6,会形成酸雨;向煤中加入适量的CaCO3(或CaO),高温下石灰石分解生成CaO,可与SO2以及氧气反应生成硫酸钙,发生的反应为:2CaCO3+2SO2+O2![]() 2CO2+2CaSO4,可以大大减少燃物产物中SO2的量,故答案为:5.6;CaCO3(或CaO);
2CO2+2CaSO4,可以大大减少燃物产物中SO2的量,故答案为:5.6;CaCO3(或CaO);
(4)明矾净水原理是硫酸铝钾溶液中含有铝离子,铝离子水解Al3++3H2O![]() Al(OH)3(胶体)+3H+,生成氢氧化铝胶体和氢离子,氢氧化铝胶体具有吸附性净水,故答案为:Al3++3H2O
Al(OH)3(胶体)+3H+,生成氢氧化铝胶体和氢离子,氢氧化铝胶体具有吸附性净水,故答案为:Al3++3H2O![]() Al(OH)3(胶体)+3H+。
Al(OH)3(胶体)+3H+。


科目:高中化学 来源: 题型:
【题目】进入秋冬季节后,雾霾这种环境污染问题逐渐凸显.从物质分类来看雾霾属于胶体,它区别于溶液等其它分散系的本质特征是( )
A.胶粒可以导电
B.胶体是混合物
C.胶体粒子大小在1~100nm之间
D.胶体的分散剂为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】真菌聚酮(X)具有多种生物活性,一定条件下可分别转化为Y和Z。

下列说法正确的是
A. X的分子式为:C18H26O5
B. X、Y和Z均能与Na2CO3溶液反应,且均有气体生成
C. X、Y和Z中均不含手性碳原子
D. 等物质的量的X、Y和Z分别与足量的NaOH溶液反应,消耗的NaOH溶液物质的量之比为1∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)具有强氧化性,可作为水处理剂和高容量电池材料。工业上生产高铁酸钾的工艺流程如下:
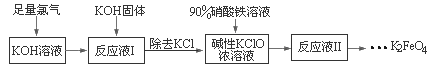
已知K2FeO4具有下列性质:①可溶于水,微溶于KOH溶液,难溶于异丙醇;②在0℃-5℃,强碱性溶液中比较稳定;③在Fe3+和Fe(OH)3催化作用下发生分解;④在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2
请完成下列填空:
(1)已知Cl2与KOH在低温下可制得KClO,请写出化学反应方程式____________。
(2)在“反应液Ⅰ”中加KOH固体的目的是____________________。
(3)生产K2FeO4的化学反应方程式为________________,制备K2FeO4时,须将Fe(NO3)3溶液缓慢滴加到碱性的KClO浓溶液中,并且不断搅拌,采用这种混合方式的原因是___________________。
(4)请补充完整由“反应液Ⅱ”得到K2FeO4晶体的实验步骤。(可选用的试剂:NaOH溶液、KOH溶液、蒸馏水和异丙醇)
① 向反应液Ⅱ中加入饱和________,在冰水浴中静置结晶后过滤,得K2FeO4粗产品;
② 将K2FeO4粗产品溶解在___________中,再次在冰水浴中静置结晶后过滤,得到较纯净的K2FeO4;
③ 将K2FeO4晶体再用少量__________洗涤,低温真空干燥,得到高铁酸钾成品。
(5)从“反应液Ⅱ”中分离出K2FeO4晶体后,可以得到的副产品有_________(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,A为银白色金属,A、B、C、D、E、F中均含有同一种元素。常温下G为液态,H为气态。
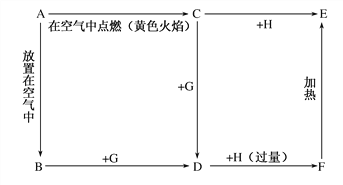
试回答:
(1)写出化学式:C________,D________,F________,H________。
(2)A与水反应的化学方程式为___________________________________________________。
(3)写出F→E的化学方程式:___________________________________________________。
(4)若向E的饱和溶液中通入足量的H,实验现象为_________________________________。
(5)写出F的一种用途___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下面的装置中,A是实验室制备Cl2的发生装置,圆底烧瓶中盛放的是二氧化锰,C、D为气体净化装置;E硬质玻璃管中装有细铁丝网;F为干燥的空广口瓶:烧杯G为尾气吸收装置。试回答:
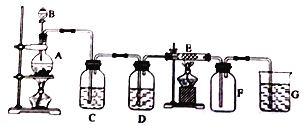
(1)C装置中试剂为______。
(2)E中的现象为______。
(3)写出在A、G中发生反应的离子方程式:A: ___________。G: ________________。
(4)KMnO4的氧化性比MnO2强得多,实验室也可以用KMnO4固体和浓盐酸反应制取氯气,反应方程式如下:2 KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
①考试用“单线桥”标出电子转移的方向和数目: __________。
②该反应中被氧化和未被氧化的HCl的物质的量之比是________,如果将20mL、12mol/L的浓盐酸与足量KMnO4充分反应,实际能收集到氯气在标准状况下的体积为_______。
A.≥1.68L B.>1.68L C.≤1.68L D.<1.68L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【福建省宁德市2017届高三毕业班第三次质量检查化学试题】 化学与生产、生活、环境密切相关。下列有关说法正确的是
A. 酸雨的pH在5.6~7.0之间 B. 向海水中加入明矾可以使海水淡化
C. 硅太阳能电池与原电池的原理相同 D. CO2和CH4均能引起温室效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示为阿伏加德罗常数,下列叙述中,正确的是( )
A. 常温常压下,16 gSO2所含的分子数为0.25NA
B. 46 gNO2与N2O4的混合气体中所含的分子数是1NA
C. 0.1 molCl2完全反应,转移电子数目一定为0.2NA
D. 0.1 molH2与Cl2的混合气体充分反应后,体系中含有共价键总数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com