
ЁОЬтФПЁП25ЁцЪБЃЌШ§жжЫсЕФЕчРыЦНКтГЃЪ§ШчЯТБэЫљЪОЁЃ
ЛЏбЇЪН |
|
|
|
УћГЦ | ДзЫс | ДЮТШЫс | бЧСзЫс |
ЕчРыЦНКтГЃЪ§ |
|
|
|
ЛиД№ЯТСаЮЪЬтЃК
(1)pHЯрЕШЕФ![]() ШмвКЁЂ
ШмвКЁЂ![]() ШмвКЁЂ
ШмвКЁЂ![]() ШмвКжаЃЌЮяжЪЕФСПХЈЖШзюаЁЕФЪЧ____________ЃЈЬюЛЏбЇЪНЃЉЁЃ
ШмвКжаЃЌЮяжЪЕФСПХЈЖШзюаЁЕФЪЧ____________ЃЈЬюЛЏбЇЪНЃЉЁЃ
(2)вбжЊ![]() ЮЊе§бЮЃЌвРОнБэИёЪ§ОнЃЌ
ЮЊе§бЮЃЌвРОнБэИёЪ§ОнЃЌ![]() ЕФЕкЖўМЖЕчРыЦНКтГЃЪ§БэДяЪН
ЕФЕкЖўМЖЕчРыЦНКтГЃЪ§БэДяЪН![]() ___________ЃЛ25ЁцЪБЃЌ5.6molЁЄL-1
___________ЃЛ25ЁцЪБЃЌ5.6molЁЄL-1![]() ШмвКЕФpH=____________ЁЃ
ШмвКЕФpH=____________ЁЃ
(3)ЯђЬхЛ§ОљЮЊ10mLЁЂ![]() ОљЮЊ
ОљЮЊ![]() molЁЄL-1ЕФ
molЁЄL-1ЕФ![]() ШмвККЭвЛдЊЫс
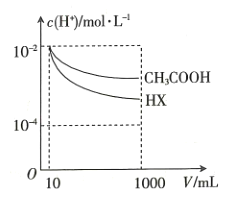
ШмвККЭвЛдЊЫс![]() ШмвКжаЃЌЗжБ№МгЫЎЯЁЪЭжС1000mLЃЌЯЁЪЭЙ§ГЬжа
ШмвКжаЃЌЗжБ№МгЫЎЯЁЪЭжС1000mLЃЌЯЁЪЭЙ§ГЬжа![]() ЕФБфЛЏШчЭМЫљЪОЃЌдђHXЕФЕчРыЦНКтГЃЪ§____________ЃЈЬюЁАДѓгкЁБЁАаЁгкЁБЛђЁАЕШгкЁБЃЉ
ЕФБфЛЏШчЭМЫљЪОЃЌдђHXЕФЕчРыЦНКтГЃЪ§____________ЃЈЬюЁАДѓгкЁБЁАаЁгкЁБЛђЁАЕШгкЁБЃЉ![]() ЕФЕчРыЦНКтГЃЪ§ЃЌРэгЩЪЧ______________________________ЁЃ
ЕФЕчРыЦНКтГЃЪ§ЃЌРэгЩЪЧ______________________________ЁЃ
(4)ГЃЮТЯТЃЌНЋ0.05molЁЄL-1ЕФАБЫЎж№ЕЮМгШы10mL0.1molЁЄL-1![]() ШмвКжажСШмвКЯджаадЃЌДЫЪБШмвКжаИїРызгХЈЖШДѓаЁЙиЯЕЮЊ_________________ЁЃ
ШмвКжажСШмвКЯджаадЃЌДЫЪБШмвКжаИїРызгХЈЖШДѓаЁЙиЯЕЮЊ_________________ЁЃ
ЁОД№АИЁП![]()
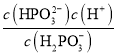 10 Дѓгк
10 Дѓгк ![]() ЯрЭЌЕФ
ЯрЭЌЕФ![]() ШмвККЭ
ШмвККЭ![]() ШмвКЯЁЪЭЯрЭЌЕФБЖЪ§ЃЌ
ШмвКЯЁЪЭЯрЭЌЕФБЖЪ§ЃЌ![]() ШмвКЕФ
ШмвКЕФ![]() БфЛЏИќДѓ
БфЛЏИќДѓ ![]()
ЁОНтЮіЁП
(1)ЫсЕФЕчРыЦНКтГЃЪ§дНаЁЃЌЫсаддНШѕЃЌдђЯрЭЌpHжЕЪБЃЌЫсЕФХЈЖШдНДѓЃЌИљОнБэИёЪ§ОнПЩжЊKa1(H3PO3) >Ka(CHCOOH)> Ka(HClO)>ЃЌЫљвдpHЯрЕШЕФШ§жжШмвКH3PO3ЕФХЈЖШзюаЁЃЛ
(2)Na2HPO3ЮЊе§бЮЃЌдђH3PO3ЮЊЖўдЊШѕЫсЃЌЦфЕкЖўМЖЕчРыЗНГЬЪНЮЊH2PO3-![]() HPO32-+H+ЃЌЦфЕчРыЦНКтГЃЪ§БэДяЪНЮЊ
HPO32-+H+ЃЌЦфЕчРыЦНКтГЃЪ§БэДяЪНЮЊ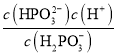 ЃЛNa2HPO3ШмвКжаДцдкзХЫЎНтЦНКтHPO32-+H2O
ЃЛNa2HPO3ШмвКжаДцдкзХЫЎНтЦНКтHPO32-+H2O![]() H2PO3-+OH-ЃЌЩшc(OH-)=aЃЌдђЦфЫЎНтЦНКтГЃЪ§ЮЊ
H2PO3-+OH-ЃЌЩшc(OH-)=aЃЌдђЦфЫЎНтЦНКтГЃЪ§ЮЊ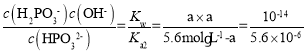 ЃЌНтЕУaдМЮЊ10-4mol/LЃЌдђШмвКжаc(H+)=10-10mol/LЃЌpH=10ЃЛ
ЃЌНтЕУaдМЮЊ10-4mol/LЃЌдђШмвКжаc(H+)=10-10mol/LЃЌpH=10ЃЛ
(3)ЫсаддНШѕЯЁЪЭЪБpHМДc(H+)БфЛЏдНТ§ЃЌОнЭМc(H+)ЯрЭЌЕФДзЫсШмвККЭHXШмвКЯЁЪЭЯрЭЌЕФБЖЪ§ЃЌHXШмвКЕФc(H+)БфЛЏИќДѓЃЌЫљвдHXЕФЕчРыЦНКтГЃЪ§ДѓгкДзЫсЕФЕчРыЦНКтГЃЪ§ЃЛ
(4)ШмвКжаДцдкЕчКЩЪиКуЃКc(NH4+)+ c(H+)=c(CH3COO-)+ c(OH-)ЃЌЖјШмвКГЪжаадЫљвдc(H+)=c(OH-)ЃЌЫљвдc(NH4+)=c(CH3COO-)ЃЌЫЎЕФЕчРыГЬЖШНЯаЁЃЌдђРызгХЈЖШДѓаЁЫГађЮЊc(NH4+)=c(CH3COO-)ЃОc(H+)=c(OH-)ЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁППЩФцЗДгІ:A(g)+B(g) ![]() C(s)+2D(g)ЕФІЄH>0,ЯТЭМЫљЪОЮЊе§ФцЗДгІЫйТЪ(v)гыЪБМф(t)ЕФЙиЯЕ,ШчЙћдкt1ЪБПЬИФБфвдЯТЬѕМў:ЂйМгШыA;ЂкМгШыДпЛЏМС;ЂлМгбЙ;ЂмЩ§ЮТ;ЂнвЦзпC,ЗћКЯЭМЪОЕФЬѕМўЪЧ(ЁЁЁЁ)ЁЃ
C(s)+2D(g)ЕФІЄH>0,ЯТЭМЫљЪОЮЊе§ФцЗДгІЫйТЪ(v)гыЪБМф(t)ЕФЙиЯЕ,ШчЙћдкt1ЪБПЬИФБфвдЯТЬѕМў:ЂйМгШыA;ЂкМгШыДпЛЏМС;ЂлМгбЙ;ЂмЩ§ЮТ;ЂнвЦзпC,ЗћКЯЭМЪОЕФЬѕМўЪЧ(ЁЁЁЁ)ЁЃ
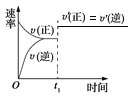
A. ЂкЂлB. ЂйЂкC. ЂлЂмD. ЂмЂн
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЙигкНКЬхЕФЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
A. вРОнЖЁДяЖћаЇгІПЩНЋЗжЩЂЯЕЗжЮЊШмвКЁЂНКЬхгызЧвК
B. ЯђЮлЫЎжаЭЖЗХУїЗЏЃЌЩњГЩФмФ§ОлаќИЁЮяЕФНКЬхЃКAl3+ЃЋ3H2O![]() Al(OH)3(НКЬх)ЃЋ3H+
Al(OH)3(НКЬх)ЃЋ3H+
C. Na+ЁЂK+ЁЂSO42-ЁЂBr-ФмдкFe(OH)3НКЬхжаДѓСПЙВДц
D. ЗаЫЎжаЕЮМгЪЪСПБЅКЭFeCl3ШмвКЃЌаЮГЩДјЕчЕФНКЬхЃЌЕМЕчФмСІдіЧП
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЛЏбЇЗДгІжаЃЌВЛЪЧбѕЛЏЛЙдЗДгІЕФЪЧЃЈ ЃЉ
A.3NO2 + H2O = 2HNO3 + NOB.2 H2+O2![]() 2H2O
2H2O
C.Cl2ЃЋH2O=HClOЃЋHClD.CuCl2ЃЋBa(OH)2=Cu(OH)2ЃЋBaCl2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПИпЬњЫсМиЃЈK2FeO4ЃЉЪЧвЛжжаТаЭЁЂИпаЇЁЂЖрЙІФмТЬЩЋЫЎДІРэМСЁЃЙЄвЕЩЯжЦБИИпЬњЫсМивдМАИпЬњЫсМиДІРэЮлЫЎЕФВПЗжСїГЬШчЯТЃК
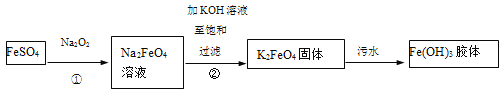
вдЯТЫЕЗЈВЛе§ШЗЕФЪЧ
A.ЂйжавЛЖЈЗЂЩњСЫбѕЛЏЛЙдЗДгІ
B.ЮлЫЎДІРэжаВњЩњFe(OH)3НКЬхЃЌЪЙаќИЁЮяОлГСЃЌРћгУСЫНКЬхОпгаНЯЧПЮќИНФмСІЕФЬиЕу
C.СэвЛжждкМюадЬѕМўЯТжЦБИK2FeO4ЕФЗДгІПЩФмЪЧЃК2Fe(OH)3+3ClOЃ=2FeO42-+3ClЃ+4H+ +H2O
D.K2FeO4ЛЙПЩвдгУгкДІРэЗЯЫЎЃЌР§ШчПЩвдАбЗЯЫЎжаЕФCNЃзЊЛЏЮЊСНжжЮоЖОЦјЬхЃЌЗДгІЙ§ГЬжаЃЌCNЃзіЛЙдМСЃЌБЛK2FeO4бѕЛЏ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП4NH3+5O2![]() 4NO+6H2OЃЌШєЗДгІЫйТЪЗжБ№гУvЃЈNH3ЃЉЁЂvЃЈO2ЃЉЁЂvЃЈNOЃЉЁЂvЃЈH2OЃЉБэЪОЃЌдђЯТСаЙиЯЕБэЪОе§ШЗЕФЪЧ ЃЈЃЉ
4NO+6H2OЃЌШєЗДгІЫйТЪЗжБ№гУvЃЈNH3ЃЉЁЂvЃЈO2ЃЉЁЂvЃЈNOЃЉЁЂvЃЈH2OЃЉБэЪОЃЌдђЯТСаЙиЯЕБэЪОе§ШЗЕФЪЧ ЃЈЃЉ
A. 5vЃЈNH3ЃЉ=6vЃЈO2ЃЉB. 5vЃЈO2ЃЉ=6vЃЈH2OЃЉ
C. 2vЃЈNH3ЃЉ=2vЃЈH2OЃЉD. 4vЃЈO2ЃЉ=5vЃЈNOЃЉ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЙигкТШЫЎЕФЫЕЗЈе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ
A. аТжЦТШЫЎКЌгаCl2ЁЂHClЁЂHClOЁЂH2OЗжзг
B. зЯЩЋЪЏШяЪдМСЕЮШыаТжЦТШЫЎжаЃЌШмвКЯШБфКьКѓБфЮоЩЋ
C. ТШЫЎКЭвКТШЖМФмЪЙИЩдяЕФгаЩЋВМЬѕЭЪЩЋ
D. аТжЦТШЫЎЕФpHжЕвЊБШОУжУТШЫЎЕФpHжЕаЁ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪЕбщЗЂЯжЃЌ298 KЪБЃЌдкТШЛЏЬњЫсадШмвКжаМгЩйСПаПСЃКѓЃЌFe3ЃЋСЂМДБЛЛЙдГЩFe2ЃЋЁЃФГЯФСюгЊаЫШЄаЁзщИљОнИУЪЕбщЪТЪЕЩшМЦСЫШчЭМЫљЪОдЕчГизАжУЁЃЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧ
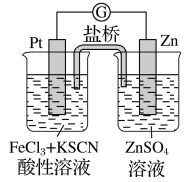
A. ИУдЕчГиЕФе§МЋЗДгІЪЧЃКZnЃ2eЃ=Zn2ЃЋ
B. зѓЩеБжаШмвКЕФКьЩЋж№НЅЭЪШЅ
C. ИУЕчГиВЌЕчМЋЩЯСЂМДгаЦјХнГіЯж
D. ИУЕчГизмЗДгІЮЊЃК3ZnЃЋ2Fe3ЃЋ=2FeЃЋ3Zn2ЃЋ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЪЕбщВйзїФмДяЕНЪЕбщФПЕФЕФЪЧ
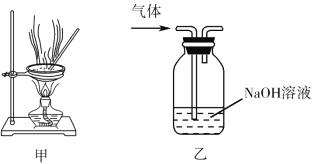
A. гУОЫЎЪЊШѓЕФpHЪджНВтСПШмвКЕФpH
B. НЋ4.0 g NaOHЙЬЬхжУгк100 mLШнСПЦПжаЃЌМгЫЎжСПЬЖШЃЌХфжЦ1.000 molЁЄL1NaOHШмвК
C. гУзАжУМзеєИЩAlCl3ШмвКжЦЮоЫЎAlCl3ЙЬЬх
D. гУзАжУввГ§ШЅЪЕбщЪвЫљжЦввЯЉжаЕФЩйСПSO2
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com