
| A. | I2 | B. | KIO3 | C. | KI |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | Cu2++2OH-═Cu(OH)2↓ CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | CO32-+2H+═CO2↑+H2O BaCO3+2HCl═BaCl2+CO2↑+H2O | |
| C. | Ca2++CO32-═CaCO3↓ Ca(NO3)2+Na2CO3═CaCO3↓+2NaNO3 | |
| D. | H++OH-═H2O Ba(OH)2+H2SO4═BaSO4+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁红属于盐类 | B. | 明矾属于碱类 | ||
| C. | SiO2属于酸性氧化物 | D. | NaHCO3属于酸类 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质 | B. | 氧化物 | C. | 无机物 | D. | 有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.4Q1+0.05Q2 | B. | 0.4Q1+0.05Q3 | C. | 0.4Q1+0.1Q3 | D. | 0.4Q1+0.2Q2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只能有一种分类标准 | B. | 分类标准不同,物质所属类别不同 | ||
| C. | 可能有多种分类标准 | D. | 一种分类标准对应一种分类结果 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
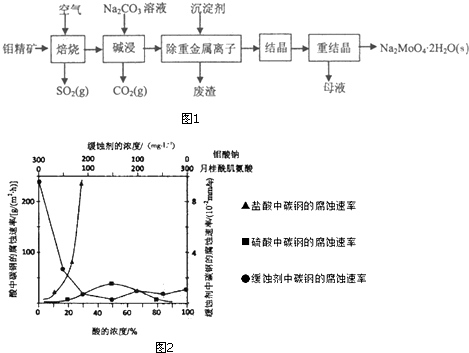
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com