
【题目】用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO等]制取CoCl2·6H2O的工艺流程如下:
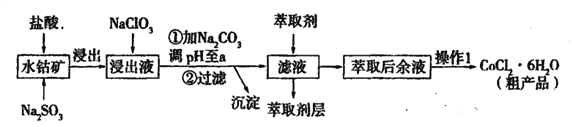
已知:①浸出液含有的阳离子主要有,H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe( OH)3 | Fe(OH)2 | Co(OH)2 | Al( OH)3 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)①浸出过程中加入Na2SO3的目的是____。
②向浸出液中加入NaClO3的离子反应方程式为____。
③为提高浸取率除了适当增大NaClO3浓度,升高温度还可采取措施____(答一条即可)。若不慎向“浸出液”中加入NaClO3过量时,可能会生成有毒气体,写出生成该有毒气体的离子方程式____。
(2)①“加Na2CO3调pH至a”,过滤所得到的沉淀成分为____。
②萃取剂对金属离子的萃取率与pH的关系如图,萃取剂的作用是____;其使用的适宜pH范围是____(填编号)。
A.2.0—2.5 B. 3.0—3.5 C.4.0—4.5 D.5.0—5.5

③“操作1”中包含的基本实验操作,它们依次是_______、____和过滤、减压烘干。
(3)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤,洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是____(答一条即可)。
【答案】 将钴元素还原到+2价 ClO3-+6Fe2++6H+=Cl-+6Fe3++3 H2O 粉碎矿石(其它合理答案均可) ClO3-+5Cl-+6H+=3Cl2↑+3H2O Fe(OH)3. Al(OH)3 除去溶液中的Mn2+ B 蒸发(浓缩) 冷却(结晶) 粗产品含有可溶性氯化物或晶体失去了部分结晶水(其它合理答案均可)
【解析】试题分析:本题以水钴矿为原料制取CoCl2·6H2O的流程为载体,考查流程的分析,离子方程式的书写,反应条件的选择,图像分析,基本实验操作和误差分析。
(1)①水钴矿中加入盐酸、Na2SO3浸取后浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等,此过程中发生的反应有:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O、Fe2O3+SO32-+4H+=2Fe2++SO42-+2H2O、Al2O3+6H+=2Al3++3H2O、MnO+2H+=Mn2++H2O,浸出过程中加入Na2SO3的目的是作还原剂,将Co元素还原到+2价,Fe元素还原为Fe2+。
②向浸出液中加入NaClO3将Fe2+氧化成Fe3+、NaClO3被还原成Cl-,反应可写成ClO3-+Fe2+→Fe3++Cl-,根据得失电子守恒配平为ClO3-+6Fe2+→6Fe3++Cl-,结合原子守恒和溶液呈酸性,写出离子方程式为ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O。
③为提高浸取率除了适当增大NaClO3浓度、升高温度,还可以采取的措施粉碎矿石、搅拌等。若不慎向“浸出液”中加入NaClO3过量,过量的NaClO3与Cl-在酸性条件下发生归中反应产生有毒的Cl2,反应的离子方程式为ClO3-+5Cl-+6H+=3Cl2↑+3H2O。
(2)①加入NaClO3反应后溶液中主要阳离子为H+、Co2+、Fe3+、Mn2+、Al3+、Na+,根据各阳离子以氢氧化物形成沉淀时的pH分析,“加Na2CO3调pH至a”是除去Fe3+、Al3+,所以过滤所得到的沉淀成分为Fe(OH)3、Al(OH)3。
②浸出液中加入Na2CO3调pH至a除去Fe3+、Al3+,此时溶液中主要阳离子为Co2+、Mn2+、Na+等,则加入萃取剂的作用是除去溶液中的Mn2+,根据图示为了除去Mn2+应使Mn2+的萃取率尽可能高、Co2+的萃取率尽可能低,则适宜的pH范围为3.0~3.5,答案选B。
③萃取后的余液中主要含Co2+、Na+、Cl-等,从萃取后的余液中获得CoCl2·6H2O的“操作1”为蒸发浓缩、冷却结晶、过滤、减压烘干(防止CoCl2·6H2O分解失去结晶水)。
(3)测定CoCl2·6H2O含量的原理:加入AgNO3溶液与Cl-反应形成AgCl沉淀,通过测定AgCl的质量计算CoCl2·6H2O的含量。粗产品中CoCl2·6H2O的质量分数大于100%的原因可能是:粗产品中含可溶性氯化物(如NaCl等)、CoCl2·6H2O晶体失去了部分结晶水。


科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列说法不正确的是
A.1 mol醋酸的质量与NA个醋酸分子的质量相等
B.NA个氧气分子和NA个氢气分子的质量比等于16∶1
C.30 g乙烷(C2H6)所含的原子数目为NA
D.在标准状况下, 0.5NA个氯气分子所占体积约是11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在500℃时,把0.3mol SO2和0.2mol O2充入一个体积为10L并盛有V2O5(催化剂)的真空密闭容器中,保持温度不变,经2min后,容器内的压强不再变化,此时容器内压强减小20%。下列说法正确的是( )
A.该温度下此反应的平衡常数K=400
B.其他条件不变,再充入0.3mol SO2和0.2mol O2平衡时,SO2的体积分数增大
C.平衡时,SO2的转化率为95%
D.前2min SO2的平均反应速率0.02mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种锂铜可充电电池,工作原理如图。在该电池中,非水系电解液和水系电解液被锂离子固体电解质陶瓷片(LISICON)隔开。下列说法不正确的是
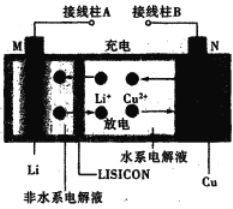
A. 陶瓷片允许Li+通过,不允许水分子通过
B. 放电时,N为电池的正极
C. 充电时,阴极反应为:Li+ +e-=Li
D. 充电时,接线柱A应与外接电源的正极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s) + CO2(g)![]() 2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:
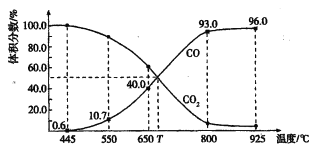
已知:气体分压(P分)=气体总压(p总)×体积分数。下列说法正确的是
A. 550℃时,若充入惰性气体,V正、V逆均减小,平衡不移动
B. 650℃时,反应达平衡后CO2的转化率为40.0%
C. T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动
D. 925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp= 23. 04p总
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中的每个编号表示一种元素,请根据要求回答问题
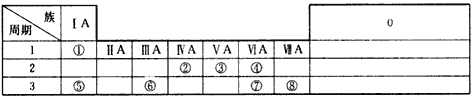
(1)⑤和⑥两种元素的原子半径大小是⑤____⑥(填“<"或“>”);
(2)由①和②两种元素组成的最简单化合物的化学式是________;
(3)⑥的单质与⑤的最高价氧化物的水化物的水溶液反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是( )
A. 用惰性电极电解1 L 1mol/L CuSO4溶液,阴极得到的铜原子的数目一定为NA
B. 将2.3g钠投入到100ml 0.8mol/L的稀盐酸中,完全反应后可得到H2的数目为0.01NA
C. 1molCl2溶于水后溶液中Cl2、HClO、ClO-、Cl-四种粒子总数为2NA
D. 标准状况下,2molNa2O2与44.8LSO2完全反应,转移的电子数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A. 无色透明溶液中: Ca2+、Cu2+、Br-、Cl-
B. 能使酚酞变红的溶液中: K+、Na+、CO![]() 、AlO
、AlO![]()
C. c(ClO-)=1mol·L-1的溶液中: Fe2+、Al3+、NO![]() 、I-
、I-
D. ![]() =0.1 mol·L-1的溶液中: NH
=0.1 mol·L-1的溶液中: NH![]() 、Mg2+、SO
、Mg2+、SO![]() 、CH3COO-
、CH3COO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在同一溶液中一定能大量共存的是( )
A. 含大量Ba2+的溶液中:Cl-、K+、SO![]() 、CO
、CO![]()
B. 含大量H+的溶液中:Mg2+、Na+、CO![]() 、SO
、SO![]()
C. 含大量OH-的溶液中:K+、NO、SO![]() 、Cu2+
、Cu2+
D. 含大量Na+的溶液中:H+、K+、SO![]() 、NO
、NO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com