
| 滴定次数 | 滴定前读数(mL) | 滴定后读数(mL) |
| 1 | 1.20 | 16.21 |
| 2 | 3.00 | 18.90 |
| 3 | 4.50 | 19.49 |
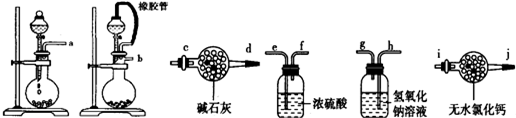
分析 I.(1)根据反应装置--干燥装置--吸收装置-尾气处理装置排序;
(2)盐酸和硝酸都具有挥发性;
(3)空气中的水和二氧化碳影响实验结果;
II.(4)酸式滴定管只能量取酸性溶液,碱式滴定管只能量取碱性溶液,根据溶液的酸碱性确定滴定管;根据滴定终点确定指示剂;滴定终点时溶液从无色变为浅红色,30s内不褪色;根据氢氧化钠和硫酸铵的关系式计算硫酸铵的量,最后再计算N元素的含量;
(5)在滴定实验结束后发现滴定用的碱式滴定管玻璃尖嘴内出现了气泡,滴定开始时无气泡,导致硫酸铵的测定结果偏小;
解答 解:I.(1)根据反应装置--干燥装置--吸收装置-尾气处理装置排序,所以其排列顺序是:b-e,f-h,g-c,
故答案为:b-e,f-h,g-c;
(2)制取二氧化碳时需要碳酸盐和酸反应,稀盐酸、浓硝酸都具有挥发性,影响实验结果,氢氧化钠和盐不能生成二氧化碳,故选B;
(3)为防止影响实验结果,需要吸收二氧化碳和水蒸气,
故答案为:防止空气中水和二氧化碳进入装置影响实验结果;
II.(4)硫酸铵属于强酸弱碱盐,其溶液呈酸性,所以需要酸式滴定管量取硫酸铵溶液,滴定终点的pH约为8.8,酚酞的变色范围是8-10,所以选取酚酞作指示剂;
滴定终点时,溶液从无色变为浅红色,30s内不褪色;
2(NH4)2SO4+6HCHO=(CH2)6N4+2H2SO4+6H2O、2NaOH+H2SO4=Na2SO4+2H2O,所以硫酸铵和NaOH的关系式为:(NH4)2SO4---2NaOH,NaOH溶液的平均体积=$\frac{(16.21-1.20)+(18.90-3.00)+(19.49-4.50)}{3}$mL=15.3mL,根据(NH4)2SO4---2NaOH得m[(NH4)2SO4]=$\frac{0.0153L×0.08mol/L}{2}$=0.0808g,0.6g硫酸铵中硫酸铵的质量=0.0808g×5=0.404g,氮元素的质量分数为$\frac{0.404g×\frac{28}{132}}{0.6g}$×100%=14%,
故答案为:酸式滴定管;酚酞;溶液从无色变为浅红色,30s内不褪色;14%;
(5)在滴定实验结束后发现滴定用的碱式滴定管玻璃尖嘴内出现了气泡,滴定开始时无气泡,导致NaOH溶液的量偏小,根据(NH4)2SO4---2NaOH得,导致测定N含量偏小,故答案为:偏小.
点评 本题考查了物质含量的测定,明确实验原理是解本题关键,根据物质间的反应结合实验操作进行解答,此种类型的题阅读量较大,同时考查书写获取信息、加工信息的能力,注意II(4)中酸碱指示剂的选取方法,注意取用的溶液为配制溶液的五分之一,不是全部溶液,为易错点.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | O2和O3互为同位素,性质相似 | |
| B. | 等质量的碳酸钠和碳酸氢钠粉末分别与足量同浓度的稀盐酸反应,前者产生的二氧化碳多,后者产生二氧化碳的速率慢 | |
| C. | 明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 | |
| D. | 浓硫酸通常可用铝槽车来运输 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaNO2是氧化剂 | |
| B. | NH4Cl中的氮元素被氧化 | |
| C. | 每生成1 mol N2转移的电子的物质的量为6 mol | |
| D. | N2既是氧化剂,又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
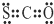
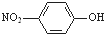
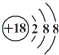

| A. | ①④⑤ | B. | ①②③④⑤ | C. | ③⑤⑥⑦ | D. | 全部正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2和N2O4组成的46g混合气体中氮原子的数目为NA | |
| B. | 1molC2H2分子中含有σ键的数目为2NA | |
| C. | HClO光照分解产生22.4LO2,转移的电子数为4NA | |
| D. | 常温下,1L0.1mol/LFe2(SO4)3溶液中阳离子数小于0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液,无CaCO3沉淀产生 | |
| B. | SO2具有漂白性,将过量SO2气体通入紫色石蕊试液时,石蕊试液先变红后褪色 | |
| C. | CO、SO2、NO2都是对大气产生污染的气体,它们的空气中都能稳定存在 | |
| D. | 类比(比较)是研究物质性质的常用办法之一,可预测许多物质的性质.例如:将SO2通入BaCl2溶液不产生沉淀,则SO2通入Ba(NO3)2溶液也不产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2既是氧化剂也是还原剂 | |
| B. | 被氧化的氯原子数是被还原的氯原子数的5倍 | |
| C. | 当有11.7 g的NaCl生成时,电子转移数为0.2NA | |
| D. | NaCl是还原产物,NaClO3是氧化产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com