
科目:高中化学 来源:2016届安徽省高三下学期冲刺模拟理综化学A卷(解析版) 题型:填空题
为治理环境,减少雾霾,应采取措施减少二氧化硫、氮氧化物(NOx)等的排放量。
Ⅰ.处理NOx的一种方法是利用甲烷催化还原NOx。
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ/mol
②CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H2=-586.7kJ/mol
(1)若用4.48LCH4还原NO生成N2,则放出的热量为______kJ。(气体体积已折算为标准状况下)
Ⅱ.(2)NOx可用强碱溶液吸收产生硝酸盐。在酸性条件下,FeSO4溶液能将NO3-还原为NO,NO能与多余的FeSO4溶液作用生成棕色物质,这是检验NO3-的特征反应。写出该过程中产生NO的离子方程式: 。
(3)用电化学处理含NO3-的废水,电解的原理如图1所示。则电解时阴极的电极反应式为 ;当电路中转移20 mol电子时,交换膜左侧溶液质量减少________g。

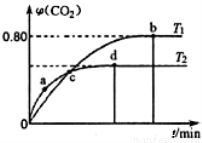
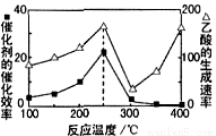
图1 图2 图3
Ⅲ.利用I2O5消除CO污染的反应为:5CO(g)+I2O5(s) 5CO2(g)+I2(s)。不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 molCO,测得CO2的体积分数(φ)随时间(t)变化曲线如图2所示。
5CO2(g)+I2(s)。不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4 molCO,测得CO2的体积分数(φ)随时间(t)变化曲线如图2所示。
(4)T1时,该反应的化学平衡常数的数值为 。
(5)下列说法不正确的是_______(填字母)。
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的压强相等
C.d点时,在原容器中充入一定量氦气,CO的转化率不变
D.b点和d点时化学平衡常数的大小关系:Kb<Kd
Ⅳ.以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4通过反应CO2(g)+CH4(g)
CH3COOH(g) △H<0直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图3所示。
(6)①250~300℃时,乙酸的生成速率减小的主要原因是 。
②工业生产中该反应的温度常选择250℃、不选择400℃,从综合经济效益考虑,其原因是 。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三5月高考模拟理综化学试卷(解析版) 题型:选择题
R、W、X、Y、Z为原子序数依次递增的同一短周期元素,m、n均为正整数,下列说法正确的是
A.离子半径:Rn+>Zm-
B.若Y的最高价氧化物对应的水化物HnYOm为强酸,则X的氢化物沸点一定比Y的氢化物的沸点低
C.若X的气态氢化物能使湿润的石蕊试纸变蓝,则标准状况下,18g Y的氢化物的体积为2.24 L
D.若R(OH)n为弱电解质,则W(OH)n+1可与KOH溶液反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二下期中文科化学试卷(解析版) 题型:选择题
我国是一个淡水资源比较匮乏的国家,右图是海水淡化原理的一种示意图,符合此原理的方法称为

A.蒸馏法 B.电渗析法
C.离子交换法 D.太阳能蒸发法
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二下期中文科化学试卷(解析版) 题型:选择题
下列各组离子,在水溶液中能大量共存的是
A.Fe3+、OH- B.Na+、SO42- C.Ag+、Cl- D.H+、OH-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南师大附中高一下期中化学试卷(解析版) 题型:选择题
已知三价铁离子的氧化性比铜离子强。现将amol铁和bmol铜的混合物与含有cmolHNO3的稀溶液充分反应,设还原产物为NO。下列结论:①若只有一种氧化产物,则3c=8a;②若只有二种氧化产物,被还原的硝酸物质的量为0.25c mol;③若有三种氧化产物,被还原的硝酸物质的量为0.25c mol;④若剩余金属0.5a mol,则氧化产物为一种或二种。其中正确的组合是
A.只有② B.①② C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南师大附中高一下期中化学试卷(解析版) 题型:填空题
某温度时,在容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析:
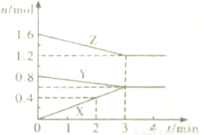
(1)该反应的化学方程式为: 。
(2)反应开始至2min末, X的反应速率为 。
(3)若要加快该反应的化学反应速率可以采取的措施有:增大物质浓度、加压、 、使用正催化剂等。
(4)反应达到平衡状态的起始时间为 min,平衡时Z的转化率为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高一下期中化学试卷(解析版) 题型:填空题
利用废旧镀锌铁皮制备磁性Fe3O4胶体粒子及副产物ZnO,制备流程图如下:
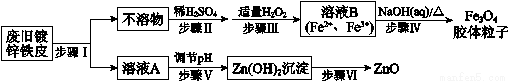
已知:Zn及其化合物的性质与Al及其化合物的性质相似,如:Zn既能溶于强酸又能溶于强碱溶液。
回答下列问题:
(1)步骤I中所用的试剂可以是_________。
(2)步骤III中加入H2O2的作用是做______________。(填“还原剂”或“氧化剂”)
(3)步骤V可选用的试剂是_______(填序号)。
a.NaOH溶液 b.氨水 c.适量HCl溶液
(4)步骤VI的实验操作是_____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北武汉华中师大一附高一下期中化学试卷(解析版) 题型:选择题
A、B、C、D四种短周期主族元素的原子序数依次减小;在短周期的主族元素中D的原子半径最大;C原子最外层电子数与电子层数相等;B元素的主要化合价:最高正价+最低负价=4。下列说法正确的是
A.A、C、D最高价氧化物对应的水化物两两之间能发生反应
B.D和A能形成原子个数比为2︰1型的离子化合物
C.最高价氧化物对应的水化物的酸性:B>A
D.C的氧化物是碱性氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com