
分析 金属阳离子和阴离子之间的化学键为离子键,一般盐、碱金属氧化物中含有离子键,非金属元素之间的化学键为共价键,其中相同非金属元素形成的为非极性共价键,不同非金属元素形成的为极性共价键,据此进行判断.
解答 解:(A)CO2 中只含共价键;(B)NaBr中只含有离子键; (C)NaOH 中既含有离子键又含有共价键; (D)Na2O2 含有非极性键的离子化合物;(E)H2O2 中既含有极性键又含有非极性键; (F)H2S 中只含共价键;(G)MgCl2 中只含有离子键; (H)NH4Cl中既含有离子键又含有共价键;
所以只含有离子键的是BG;只有共价键的是AEF;既含有离子键又含有共价键的是CDH;含有非极性键的是DE;既含有极性键又含有非极性键的是E,
故答案为:BG;AEF;CDH;DE;E.
点评 本题考查了化学键的判断,明确哪些元素之间易形成离子键或共价键是解本题关键,题目难度不大.


 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 2 L氟化氢气体分解成1L氢气与1L氟气吸收270kJ热量 | |
| B. | 1mol氢气与1mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ | |
| C. | 在相同条件下,1mol氢气与1 mol氟气的总能量大于2mol氟化氢气体的能量 | |
| D. | 1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该反应是吸热反应 | |
| B. | 断裂1 mol H-H键和1 mol Cl-Cl键时能放出x kJ能量 | |
| C. | 断裂2 mol H-Cl键需要吸收y kJ的能量 | |
| D. | 2 mol HCl(g)的总能量高于1 molH2(g)和1 mol Cl2(g)的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式可以表示为CH2CH2 | |
| B. | 甲烷和苯都能发生取代反应 | |
| C. | 乙醇、乙烷和乙酸都可以与钠反应生成氢气 | |
| D. | 石油的分馏和煤的干馏都是物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
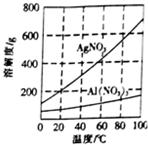 实验室中利用含银废料(主要含有AgNO3和AgCl)制取硝酸银的实验步骤如下:
实验室中利用含银废料(主要含有AgNO3和AgCl)制取硝酸银的实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
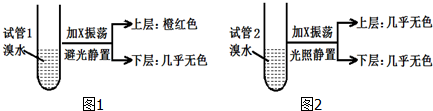
| A. | 相同条件下,X的密度比水小 | |
| B. | X的同分异构体共有5种 | |
| C. | X与溴水因发生加成反应而使溴水褪色 | |
| D. | 实验后试管2中的有机层在上层还是下层,可通过加水确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
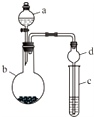 某课外小组同学设计了如图所示装置(夹持、加热仪器省略)进行系列实验.请根据下列实验回答问题:
某课外小组同学设计了如图所示装置(夹持、加热仪器省略)进行系列实验.请根据下列实验回答问题: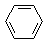 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$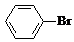 +HBr.能证明该反应是取代反应,而不是加成反应的操作和现象取反应后上层清液加硝酸银溶液,产生浅黄色沉淀.
+HBr.能证明该反应是取代反应,而不是加成反应的操作和现象取反应后上层清液加硝酸银溶液,产生浅黄色沉淀.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
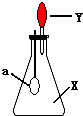 如图中,锥形瓶内盛有气体X,滴管内盛有液体Y.若挤压滴管胶头,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓起.气体X和液体Y不可能是( )
如图中,锥形瓶内盛有气体X,滴管内盛有液体Y.若挤压滴管胶头,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓起.气体X和液体Y不可能是( )| A. | X是NH3,Y是水 | B. | X是SO2,Y是KOH浓溶液 | ||
| C. | X是CO2,Y是稀盐酸 | D. | X是HCl,Y是NaCl稀溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com