
【题目】某学习小组的同学对氯气与铁的反应及产物进行了如下探究:
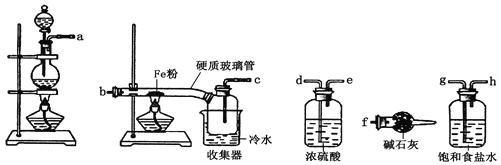
(1) 装置的连接顺序为a→_____→____→____→____→b→c→f。
(2) 硬质玻璃管中可观察到的现象是___________________;硬质玻璃管与收集器之间没有用导管连接,原因是____________________;反应一段时间、熄灭酒精灯,冷却后,将收集器及硬质玻璃管中物质快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:

(3) 试剂X的化学式为___________;有同学分析淡黄色溶液中含有Fe2+,你认为_______(填“合理”或“不合理”);固体产物的成分可能为__________(填相应的字母);
A Fe和FeCl3 B FeCl2和FeCl3 C Fe、FeCl2和FeCl3 D Fe和FeCl2
(4) 加入少许植物油的作用是___________________,用离子方程式表示加入新制氯水后溶液红色加深的原因_______________________________。
(5) 某小组同学实验时在加入新制氯水后,并未得到深红色溶液,请帮助他们分析原因________,请设计实验对你所分析的原因进行验证,简要写出实验方案___________
(6)Cl2是一种黄绿色有刺激性气味的气体,实验室通常用NaOH溶液来吸收Cl2,以减少环境污染。若实验时需要450mL 4mol/L的NaOH溶液,则配制时,需要用托盘天平称取NaOH的质量为_______g,所使用的仪器除托盘天平、胶头滴管、玻璃棒外,还必须有_________。配制该溶液时,下列操作会使溶液浓度偏高的是___________。(填字母)
A 称量固体时动作缓慢 B 容量瓶未干燥立即用来配制溶液
C NaOH固体溶解后立刻转移 D 在容量瓶中定容时俯视容量瓶刻度线
E 定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
【答案】g h d e 有棕黄色的烟生成 防止堵塞 KSCN(或NH4SCN)溶液 合理 A 隔绝空气,防止Fe2+被氧化 2Fe2++Cl2=2Fe3++2Cl-、Fe3++SCN-=Fe(SCN)3 新制氯水将SCN-氧化 取少量褪色后的溶液于试管中,再滴加几滴KSCN(或NH4SCN)溶液,若溶液变红,则原因分析成立 80.0 500mL容量瓶、烧杯 CD
【解析】
(1)排列顺序为气体的制取→洗气→干燥→氯气和铁的反应→尾气处理;
(2)Fe在氯气中燃烧生成棕黄色烟,导气管口较细,易堵塞;
(3)Fe3+用KSCN溶液检验,Fe3+和KSCN反应生成络合物硫氰化铁而使溶液呈血红色;Fe和稀盐酸、氯化铁反应生成FeCl2;
(4)Fe2+不稳定而易被氧化;Fe2+被氯气氧化生成Fe3+,从而增大Fe3+浓度;
(5)Fe3+和KSCN反应生成络合物硫氰化铁而使溶液呈血红色,氯水具有强氧化性,能氧化还原性物质,如果Fe3+和KSCN混合溶液中加入氯水后未得到深红色溶液,说明溶液中硫氰化铁浓度未变大;
(6)根据配制一定物质的量浓度的溶液操作过程分析。
(1)浓硫酸具有吸水性能作氯气干燥剂、碱石灰具有碱性而吸收氯气、饱和食盐水吸收氯化氢而抑制氯气溶解,装置排列顺序为气体的制取→洗气→干燥→氯气和铁的反应→尾气处理,所以装置连接顺序为a→g→h→d→e→b→c→f,
故答案为:g;h;d;e;
(2)Fe在氯气中燃烧生成棕黄色烟,所以看到的现象是有棕黄色烟生成;棕黄色烟冷却易生成固体,导气管口较细,易堵塞,所以硬质玻璃管与收集器之间没有用导管连接,
故答案为:有棕黄色烟生成;防止堵塞;
(3)Fe3+用KSCN溶液检验,Fe3+和KSCN反应生成络合物硫氰化铁而使溶液呈血红色,所以试剂X为KSCN溶液;固体和氯气反应时可能没有完全反应,导致Fe和稀盐酸、氯化铁反应生成氯化亚铁,Fe和稀盐酸反应生成FeCl2,所以分析合理,固体中成分为Fe和FeCl3,
故答案为:KSCN;合理;A;
(4)Fe2+不稳定,易被空气中氧气氧化,所以植物油的作用是隔绝空气防止Fe2+被氧化;Fe2+被氯气氧化生成Fe3+,从而增大Fe3+浓度,Fe3+、SCN-反应生成Fe(SCN)3,从而增大络合物浓度,溶液颜色加深,涉及的反应方程式为2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3,
故答案为:隔绝空气,防止Fe2+被氧化; 2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3;
(5)Fe3+和KSCN反应生成络合物硫氰化铁而使溶液呈血红色,氯水具有强氧化性,能氧化还原性物质,如果Fe3+和KSCN混合溶液中加入氯水后未得到深红色溶液,说明溶液中硫氰化铁浓度未变大,则可能原因是新制氯水将SCN-氧化;其检验方法是:取少许褪色后的溶液于试管中,再滴加几滴KSCN溶液,若溶液变红,则原因分析成立,
故答案为:新制氯水将SCN-氧化;取少许褪色后的溶液于试管中,再滴加几滴KSCN溶液,若溶液变红,则原因分析成立;
(6)实验时需要450mL 4mol/L的NaOH溶液,需要取用500mL容量瓶中配制,配制溶液需要天平称量固体质量,精确到0.1g,依据m=nM计算需要的氢氧化钠溶质的质量=0.5L×4mol/L×40g/mol=80.0g,若实验时需要450mL 4mol/L的NaOH溶液,需要取用500mL容量瓶中配制,所使用的仪器除托盘天平、胶头滴管、玻璃棒外,还含有烧杯和500mL容量瓶,
A.称量固体时动作缓慢,可能导致氢氧化钠吸收水蒸气和空气中的二氧化碳,导致溶质减小,测定结果偏低,故A错误;
B.最后配制溶液需要加入水定容,容量瓶未干燥立即用来配制溶液对配制溶液的结果无影响,故B错误;
C.NaOH固体溶解后溶液温度升高,立刻转移溶液温度升高,常温下液面未达到刻度,溶液浓度增大,故C正确;
D.在容量瓶中定容时俯视容量瓶刻度线,定容未达到刻度,溶液浓度增大,故D正确;
E.定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线,水加入超出刻度线,溶液浓度减小,故E错误;
故选CD。


科目:高中化学 来源: 题型:
【题目】下列反应中,氧化剂与还原剂物质的量的关系不是1∶2的是
A.O3+2KI+H2O===2KOH+I2+O2
B.3NO2+H2O===2HNO3+NO
C.3S+6NaOH===Na2SO3+2Na2S+3H2O
D.4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.用药匙取用粉末状或小颗粒状固体
B.pH试纸使用时不需要润湿,红色石蕊试纸检测气体时也不需要润湿
C.蒸馏时蒸馏烧瓶中的液体尽量多些,加沸石进行蒸馏,但液体也不能蒸干
D.分液时下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A. NaHCO3(s) ![]() Na2CO3(s)
Na2CO3(s) ![]() NaOH(aq)
NaOH(aq)
B. Al(s)![]() NaAlO2(aq)
NaAlO2(aq)![]() Al(OH)3(s)
Al(OH)3(s)
C. AgNO3(aq)![]() [Ag(NH3)2]+(aq)
[Ag(NH3)2]+(aq)![]() Ag(s)
Ag(s)
D. Fe2O3(s)![]() Fe(s)
Fe(s)![]() FeCl3(aq)
FeCl3(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛、铬、铁、镍、铜等金属及其化合物在工业上都有重要用途。
(1)基态钛原子外围电子的轨道表达式为_____。与钛同周期的元素中,基态原子的未成对电子数与钛原子相同的有_____种。
(2)TiCl4是氯化法制取钛的中间产物。TiCl4和SiC14在常温下都是液体,分子结构相同。采用蒸馏的方法分离TiCl4和SiCl4的混合物,先获得的馏分是_____(填化学式)。
(3)[Cr(C2O4)2(H2O2)]也是铬的一种化合物,该化合物属于离子化合物,其中除含离子键、共价键外,还含有_____键。
(4)雷氐盐(Reinecke salt)的化学式为NH4[Cr(NCS)4(NH3)2] H2O,是一种易溶于水和乙醇的暗红色固体。
①雷氏盐中铬元素的化合价为_____。
②NCS的立体构型是_____,其中碳原子的杂化轨道类型为_____。
③SO2、CO2、BeCl2、SCl2四种分子中,与NCS-互为等电子体的有_____(填化学式)。
(5)Ni和La的合金是目前使用广泛的储氢材料,具有容量大、寿命长、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。

①晶体的化学式为_____。
②该晶胞的密度为dgcm-3。设NA为阿伏加德罗常数的值,则该晶胞的体积是____(用含d、NA的代数式表示)cm3。
③该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子时比较稳定。已知: a=511pm,c=397pm;标准状况下,氢气的密度为8.98X10-5 g, ![]() ,若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为_____(保留整数)。
,若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为_____(保留整数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某化合物M(仅含三种短周期元素)是一种储氢材料。为探究M的组成和性质,设计并完成如下实验:
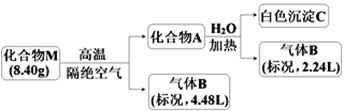
已知:化合物A仅含两种元素;气体B能使湿润的红色石蕊试纸变蓝。
请回答:(1)化合物M的组成元素是______________(用元素符号表示)。
(2)化合物A与水反应的化学方程式是______________________。
(3)镁带在足量气体B中燃烧可生成化合物M和一种单质气体,该反应的化学方程式是______。
II.无机盐X仅由三种短周期元素组成,其相对分子质量为238,原子个数比为1︰1︰4。将23.8gX与水共热,生成一种有特殊臭味的气体单质A和某强酸的酸式盐溶液B,B的焰色反应呈黄色,在溶液B中加入足量的BaCl2溶液,产生46.6g白色沉淀。请推测并回答:
(4)单质A有很强的氧化性,可用于净化空气,饮用水消毒等。A中组成元素的简单离子结构示意图为___________________________。
(5)X的化学式_____________。
(6)实验室可通过低温电解B溶液制备X。该电解反应的化学方程式___________________。
(7)X氧化能力强,对环境友好,可用于脱硝、脱硫。在碱性条件下,X氧化NO的离子方程式_____________________。
(8)X溶液与铜反应时先慢后快。某同学认为除反应放热这一因素外,还有一种可能是反应生成的Cu2+对后续反应起催化作用,为此他设计了如下实验方案:取少量铜粉置于试管中,先加入少量CuSO4溶液,再加入X溶液,振荡,观察现象。若加入硫酸铜溶液的反应快,说明Cu2+起了催化作用,反之Cu2+不起作用。写出X与铜反应的化学方程式________,判断该同学设计的验证方法合理性并说明理由_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列曲线中,纵坐标表示生成氢氧化铝的量,横坐标表示加入试剂的体积。从下边图中选出选项:
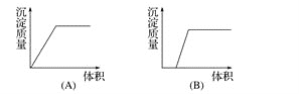
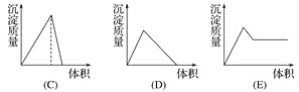
(1)向盐酸酸化的氯化铝溶液中逐滴滴入氨水至过量__________。
(2)向氢氧化钠与偏铝酸钠混合液中通入二氧化碳过量__________。
(3)向氨水中逐滴滴入氯化铝溶液至过量__________。
(4)向氯化铝溶液中滴加氢氧化钠至过量__________。
(5)向偏铝酸钠溶液滴加盐酸至过量______________。
(6)向氯化镁和氯化铝混合液中加氢氧化钠至过量____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是用铁铆钉固定两个铜质零件的示意图,若该零件置于潮湿空气中,下列说法正确的是
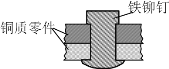
A.发生电化学腐蚀,铜为负极,铜极产生H2
B.铜易被腐蚀,铜极上发生还原反应,吸收O2
C.铁易被腐蚀,铁发生氧化反应,Fe-2e-=Fe2+
D.发生化学腐蚀:Fe + Cu2+ = Cu + Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下列氧化还原反应:
Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O。
(1)该反应的还原剂是________,还原产物是________。
(2)该反应中氧化剂与氧化产物的物质的量之比是________。
(3)当有2 mol HNO3参加反应时,被氧化的物质是________ g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com