
元素及其化合物在生产、生活中具有广泛的用途。
Ⅰ.铬化学丰富多彩.
(1)在常温下,铬能缓慢与稀硫酸反应,生成蓝色溶液。 与铜相比,其金属活泼性 (填“强”或“弱”);
⑵Cr( OH)3和Al( OH)3类似,也是两性氢氧化物,在水中存在酸式和碱式电离平衡,其酸式电离方程式是 ;
⑶工业上净化处理铬污染方法之一是:将含K2Cr2O7酸性废水放人电解槽内,加入适量的NaCl,以Fe和石墨为电极进行电解。经过一段时间后,生成Cr(OH)3和Fe(OH)3沉淀除去(已知KsP[ Fe(OH)3]=4.0×10-38,KsP[Cr(OH)3]=6.0×l0-31)。已知电解后的溶液中c( Fe3+)为2.0×10-13mol/L,则溶液中c(Cr3+)为 mol/L。
Ⅱ.物质A~H有如图所示转化关系(部分生成物未列出)。A、E、F、G均为气体,D为金属单质。
请回答下列问题:
(1)A的电子式为 D的化学式 ,C溶液的名称是 。
(2)反应①的化学方程式为 ;
反应③的离子方程式为 。
Ⅰ(1)强(1分) (2)Cr(OH)3 H++CrO2-+H2O (2分)
H++CrO2-+H2O (2分)
(3)3.0×10-6mol?L?1
Ⅱ(1) 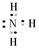 ;Ag(1分);银氨溶液(2分)
;Ag(1分);银氨溶液(2分)
(2)4NH3+5O2 4NO+5H2O (2分);3Ag+4H++NO3?=3Ag++2H2O+NO↑(2分)
4NO+5H2O (2分);3Ag+4H++NO3?=3Ag++2H2O+NO↑(2分)
解析试题分析:Ⅰ(1)在常温下,铬能缓慢与稀硫酸反应,生成蓝色溶液,说明铬的活泼性大于氢,所以铬的活泼性强于铜。
(2)酸式电离生成H+,所以电离方程式为:Cr(OH)3 H++CrO2-+H2O
H++CrO2-+H2O
(3)[c(OH?)]3= KsP[ Fe(OH)3]÷c(Fe3+)=4.0×10-38÷2.0×10-13=2.0×10-25,c(Cr3+)= KsP[Cr(OH)3]÷[c(OH?)]3=6.0×l0-31÷2.0×10-25 =3.0×10-6mol?L?1
Ⅱ(1)C溶液与葡萄糖反应生成金属D,则C溶液为银氨溶液,D为Ag,根据框图可知:A为NH3,B为AgNO3,E为O2,F为NO,G为NO2,H为HNO3。NH3的电子式为: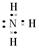
(2)反应①为氨的催化氧化,化学方程式为:4NH3+5O2 4NO+5H2O;反应③为Ag与稀硝酸的反应,离子方程式为:3Ag+4H++NO3?=3Ag++2H2O+NO↑。
4NO+5H2O;反应③为Ag与稀硝酸的反应,离子方程式为:3Ag+4H++NO3?=3Ag++2H2O+NO↑。
考点:本题考查金属活泼性的判断、方程式的书写、KsP的计算、物质的推断。


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:单选题
已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑。A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )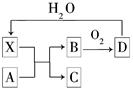
| A.X使蔗糖变黑的现象主要体现了X的强氧化性 |
| B.若A为铁,则足量A与X在室温下即可完全反应 |
| C.若A为碳单质,则将C通入少量的澄清石灰水中,一定可看到白色沉淀 |
| D.工业上,B转化为D的反应条件为高温、常压、使用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图表示常见元素单质及化合物相应关系,某些生成物已略去。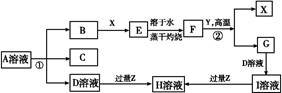
已知:反应①为氯碱工业的基础反应;X、Y为常见金属,Z为形成酸雨的主要成分。请回答下列问题:
(1)D的电子式 ;H为 (填化学式)。
(2)完成下列方程式:
①空气中含量最高的气体与C反应的化学反应方程式 ;
②反应②的化学反应方程式 ;
③足量B通入H溶液的离子反应方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下列转化关系中,X、Y是生活中用途广泛的两种金属单质,A、B是氧化物,A呈红棕色,C、D、E是中学常见的三种化合物。分析转化关系回答问题: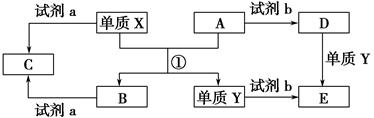
(1)请写出反应①的化学方程式_____________________________________。
(2)检验D溶液中Y离子的方法是__________________________________。
(3)若试剂a是NaOH溶液,写出单质X与NaOH溶液反应的离子方程式______________________________。
(4)若试剂b是H2SO4,工业上用E、H2SO4和NaNO2为原料制取高效净水剂Y(OH)SO4,已知还原产物为NO,则该反应的化学方程式是________________________________________。
(5)工业上电解熔融的B制取X时,若阳极产生的气体在标准状况下的体积为33.6 m3,则阴极产物的质量为________kg。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下图所示的物质转化关系中,各物质均为短周期主族元素组成的单质或化合物。已知:A、C、D、F、K均为单质;C、E、F、G、K常温下是气体,且K为工业上制造漂白粉的原料之一;J为白色沉淀且既能溶于B的水溶液,又能溶于E的水溶液;B、G可以使湿润的红色石蕊试纸变蓝;反应④是工业制化肥的重要反应之一。(图中部分反应条件及物质未列出)
请回答下列问题:
(1)B的电子式为 。
(2)H的化学式为 。
(3)写出反应④的化学方程式 。
(4)写出反应⑤的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质。气体B与气体C相遇产生大量的白烟生成E,A是强碱,D的焰色为紫色 (部分反应物和生成物及水已略去)。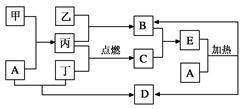
请回答下列问题
(1)写出工业制备B的化学方程式_____________________________________;
(2)写出常温下,A与丁反应的离子方程式________________________________;
(3)下图装置为用排空气法收集气体的实验装置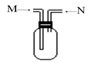
Ⅰ.当从M端通入气体时,可收集的气体有 ;
Ⅱ.当从N端通入气体时,可收集的气体有 ; (填数字编号)
①气体乙 ②气体丙 ③气体丁 ④气体B ⑤气体C
(4)E中所含阳离子的检验方法为(包括实验步骤、现象及结论) ;
(5)A中所含阳离子的检验方法为(包括实验步骤、现象及结论) 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某些化学反应可用下式表示:A+B→C+D+H2O
请回答下列问题(反应可以是固体之间的反应,也可以是在水溶液中进行的反应):
(1)若A是非金属气态单质,反应后所得溶液常用于消毒、杀菌。则A为 (填化学式下同)。反应的化学方程式为 。
(2)若A为非金属固态单质,C、D均为气体且都能使澄清石灰水变浑浊。则A为 。反应的化学方程式为 。
(3)若A为紫红色金属,D为有色气体。则A为 。反应的离子方程式为 。
(4)若A为烧碱溶液,C是相对分子质量为100的白色沉淀,D为正盐。则C为 。反应的离子方程式为 。
(5)若A、B为固体,C的水溶液能使酚酞溶液变为红色。实验室常用此反应制备C气体。则C为 。反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。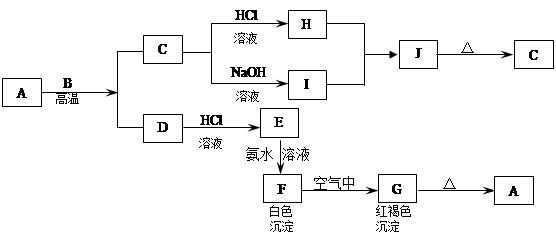
(1)A的化学式是 。
(2)F在空气中转化为G的化学方程式: 。
(3)C转化为I的离子方程式: 。
(4)D转化为E的离子方程式: 。
(5)D在高温下和水蒸气反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图所示,已知: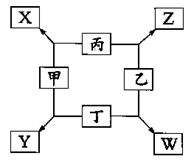
①甲、乙、丙、丁均为前三周期元素的单质,甲、乙、 丙常温下为气体。
②在一定条件下甲与丙和甲与丁都按物质量之比l:3反应,分别生成X和Y,在产物中元素甲呈负价。
③在一定条件下乙与丙和乙与丁都按物质的量之比1:2反应,分别生成Z和W,在产物中元素乙呈负价。
请填空:
(1)W的电子式为 ;
(2)X与乙催化氧化的化学方程式是______________________________________________;
(3)Y与Z反应的化学方程式是_____________________________________________;
(4)2.4g丁与足量的乙反应生成W放出QkJ的热,则该反应的热化学方程式为 ;
(5)实验室制取丙的离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com