
| A�� | O2��S2O32-����������Fe2+�ǻ�ԭ�� | |
| B�� | ÿ����1 mol Fe3O4����ת�Ƶ�����Ϊ2 mol | |
| C�� | �μӷ�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ1��1 | |
| D�� | ����2 mol Fe2+����������Fe2+��ԭ��O2Ϊ0.5mol |
���� 3Fe2++2S2O32-+O2+4OH-=Fe3O4+S4O62-+2H2O�У�FeԪ�صĻ��ϼ���+2������Ϊ+3�ۣ�SԪ�صĻ��ϼ����ߣ�ֻ��������OԪ�صĻ��ϼ۽��ͣ�ÿ����1molFe3O4��FeO•Fe2O3����OԪ�صĻ��ϼ۱仯��֪��ת�Ƶ�����Ϊ1mol��2����2-0��=4mol����÷�Ӧ��ת��4e-���Դ������
��� �⣺A��Fe��SԪ�صĻ��ϼ����ߣ�OԪ�صĻ��ϼ۽��ͣ���O2����������S2O32-��Fe2+�ǻ�ԭ������A����
B��ÿ����1molFe3O4��FeO•Fe2O3����OԪ�صĻ��ϼ۱仯��֪��ת�Ƶ�����Ϊ1mol��2����2-0��=4mol����B����
C��O2����������S2O32-��Fe2+�ǻ�ԭ�����ɷ�Ӧ�еĻ�ѧ��������֪��3molFe2+����1mol��������������μӷ�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ1����2+2��=1��4����C����
D������2molFe2+���������ɵ����غ��֪����Fe2+��ԭ��O2Ϊ$\frac{2mol����3-2��}{2����2-0��}$=0.5mol����D��ȷ��
��ѡD��
���� ���⿼��������ԭ��Ӧ��Ϊ��Ƶ���㣬���շ�Ӧ��Ԫ�صĻ��ϼ۱仯Ϊ���Ĺؼ������ص���ת�Ƽ������غ�Ŀ��飬ע��ѡ��DΪ�����״��㣬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Һ��c��H+����10-7 mol•L-1ʱ����pH��7����Һ�������� | |
| B�� | ����Һ��c��H+����10-7 mol•L-1ʱ����pH��7����Һ���ּ��� | |
| C�� | ����Һ��c��H+��=c��OH-����10-7 mol•L-1ʱ����pH��7����Һ�������� | |
| D�� | ����Һ��c��H+��=c��OH-����10-7 mol•L-1ʱ����pH��7����Һ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
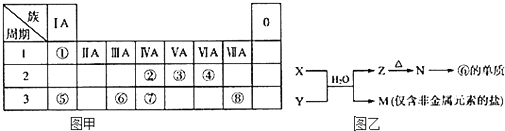
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �⻯���ͨʽΪ RH5 | B�� | ����ϼ���+5 �� | ||
| C�� | �ǽ��������ϵ��µ��� | D�� | ����ۺ������Ϊǿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
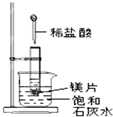 ��ͼ��ʾ�����Թܷ���ʢ�� 25��ʱ����ʯ��ˮ���ձ��У��Թ��п�ʼ���뼸С��þƬ�����õιܵ��� 5mL �������Թ��У��Իش��������⣺
��ͼ��ʾ�����Թܷ���ʢ�� 25��ʱ����ʯ��ˮ���ձ��У��Թ��п�ʼ���뼸С��þƬ�����õιܵ��� 5mL �������Թ��У��Իش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �����ܱ������п��淴ӦA2��g��+3B2��g��?2AB3��g����̽����һ�����ı�����£���������ƽ��״̬�ĸı䣬�õ���ͼ��ʾ�����ߣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ����������ж���ȷ���ǣ�������
�����ܱ������п��淴ӦA2��g��+3B2��g��?2AB3��g����̽����һ�����ı�����£���������ƽ��״̬�ĸı䣬�õ���ͼ��ʾ�����ߣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ����������ж���ȷ���ǣ�������| A�� | �����������ʹ״̬d��Ϊ״̬b | |
| B�� | ��T1��T2�����淴Ӧһ���Ƿ��ȷ�Ӧ | |
| C�� | �ﵽƽ��ʱA2��ת���ʴ�СΪ��b��a��c | |
| D�� | ��T2��n��A2������ʱ�ﵽƽ�⣬AB3�����ʵ�����СΪ��c��b��a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ƾ��͵�ˮ | B�� | ˮ�ͱ� | C�� | Һ��ͱ� | D�� | �Ҵ������Ȼ�̼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2���������ԣ�������Ư��ֽ�� | B�� | NH4HCO3���е�Ԫ�أ����������� | ||
| C�� | Fe2��SO4��3������ˮ����������ˮ�� | D�� | Al2O3Ӳ�ȴ��������²��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
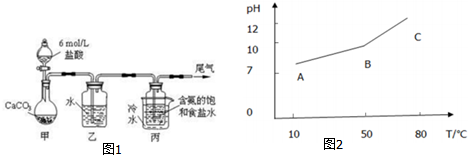
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com